脑瘤复发后的二次治疗抉择:二次手术可行性深度探讨
41 岁的凯茜未曾料想,在经历胼胝体肿瘤开颅手术之后,仅仅 4 年时间肿瘤便再次复发。而这一次,她通过全神经内镜技术成功实现肿瘤全切,术后 2 年随访结果显示肿瘤无复发迹象。INC 国际神经内镜领域专家施罗德教授,擅长将神经内镜技术与病理解剖变化巧妙结合,借助脑积水导致的脑室扩张或肿瘤占位效应形成的腔隙,构建独特的 "病理适应性手术空间"。
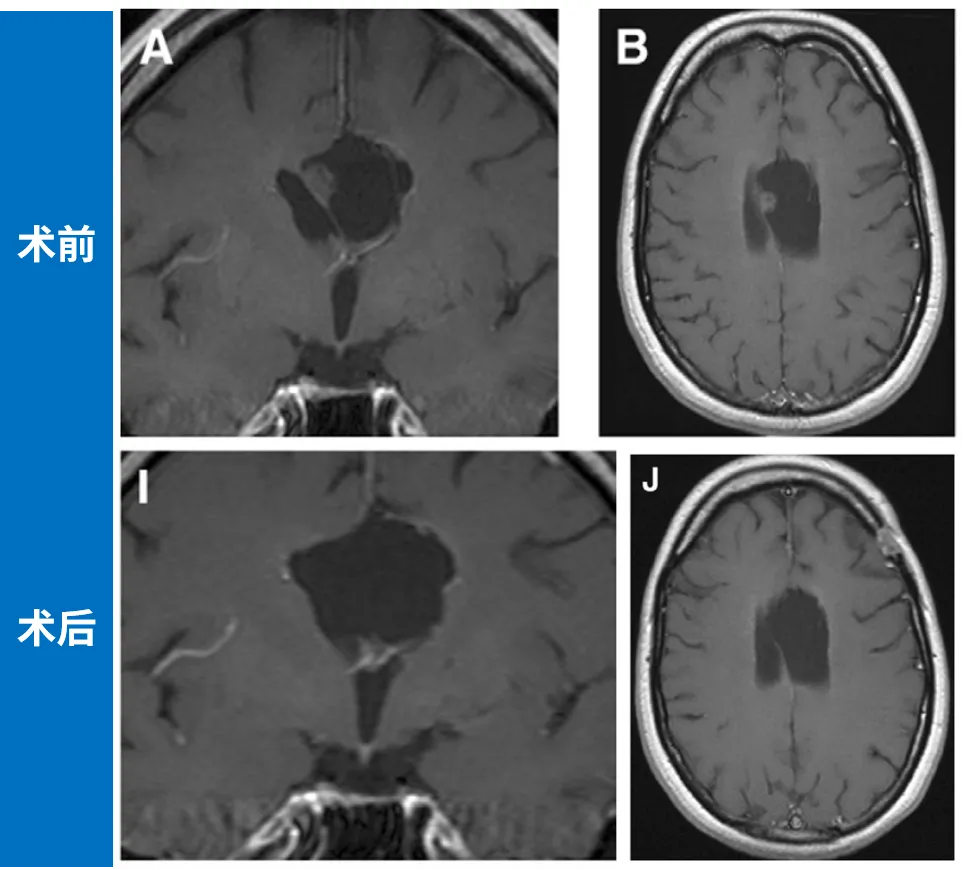
(A,B)磁共振影像清晰显示附着于透明隔的病灶;(I,J)术后 2 年 MRI 检查证实肿瘤已被完全切除。
神经内镜技术在脑室内肿瘤治疗中的显著优势
脑室内肿瘤的理想治疗策略当属神经内镜手术。这类肿瘤常常阻塞脑脊液循环通路,引发脑室扩张,从而为内镜操作提供了天然的手术空间。手术的关键在于首先精准阻断肿瘤血供,之后再根据肿瘤的具体特性,灵活选择分块切除或整体剥离的方式。
个性化手术入路设计要点:
当出现单侧脑积水时,采用偏外侧钻孔的方式优化室间孔入路;
对于第三脑室前部肿瘤,选择冠状缝钻孔;若为后部肿瘤,则需前移入口以建立直线通道;
针对压迫导水管的松果体区肿瘤,必须同步实施第三脑室造瘘术与肿瘤切除术。
神经内镜技术的精妙之处在于,既能彻底切除肿瘤,又能同步重建脑脊液循环通路,以更小的创伤实现更佳的治疗效果,尤其对于小型肿瘤可实现完全切除。
复发性神经细胞瘤的神经内镜切除典型案例
一位 41 岁女性患者,在胼胝体肿瘤显微外科手术后 4 年,随访检查发现神经细胞瘤复发。鉴于显微外科手术入路更为复杂、侵入性更强且风险更高,INC 国际神经外科医生集团旗下世界神经外科顾问团(WANG)成员、世界神经外科学会联合会(WFNS)内镜委员会前主席 Henry W.S. Schroeder 教授(施罗德教授)决定采用全内镜技术进行肿瘤切除。
神经细胞瘤的全面医学解析
病因与发病机制
神经细胞瘤的细胞起源可能为具有双向分化潜能的神经胶质前体细胞,位于侧脑室室管膜下区的室周器官。
遗传学特征
无明确的复发性染色体改变,多数病例的基因组拷贝数分析结果呈二倍体;
个别病例报道显示存在 MYCN 基因扩增现象,同时 WNT 信号通路相关基因呈现过表达;
不伴随 1p/19q 联合缺失情况,目前甲基化分型尚无法准确区分典型与非典型中枢神经细胞瘤。
预后与预测因素
生存数据统计:5 年总生存率可达 96%,10 年总生存率为 82%;
关键影响因素:
手术切除程度:全切除效果优于次全切除(但近期研究表明两者在生存率上无统计学差异);
增殖活性指标:Ki-67 (MIB1) 标记指数>4% 的患者,2 年无进展生存率为 48%;Ki-67 (MIB1)≤4% 的患者,2 年无进展生存率可达 90%(对于高 Ki-67 指数患者,需考虑辅助治疗,但最佳阈值尚未达成统一)。

神经内镜切除肿瘤的技术流程与设备应用详解
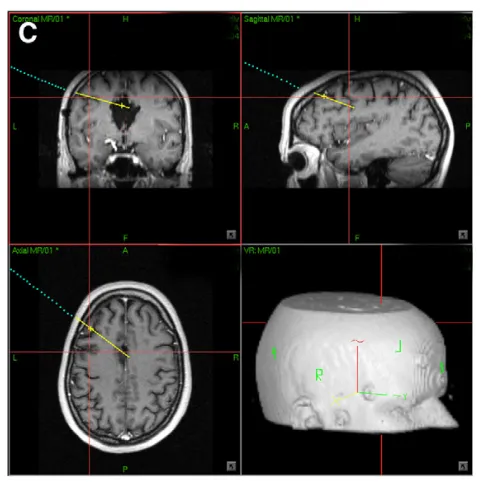
(C)神经导航手术入路规划过程
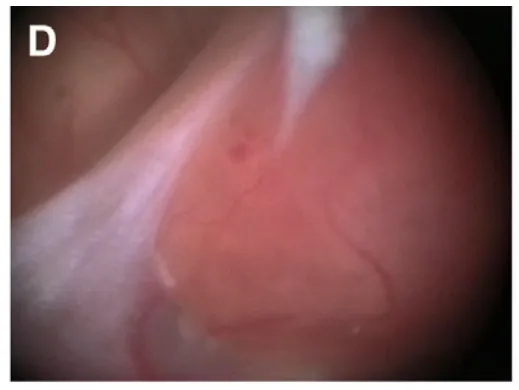
(D)显示肿瘤附着于透明隔;
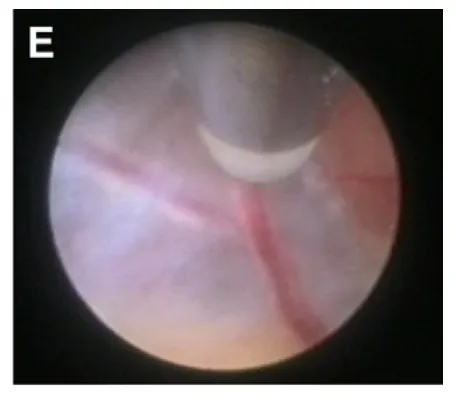
(E)在肿瘤边缘附近对透明隔进行电凝处理;
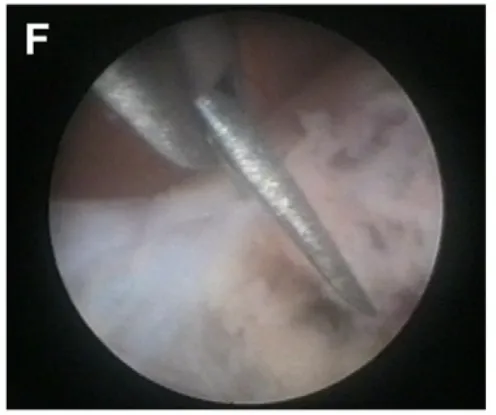
(F)沿肿瘤周围切割透明隔;
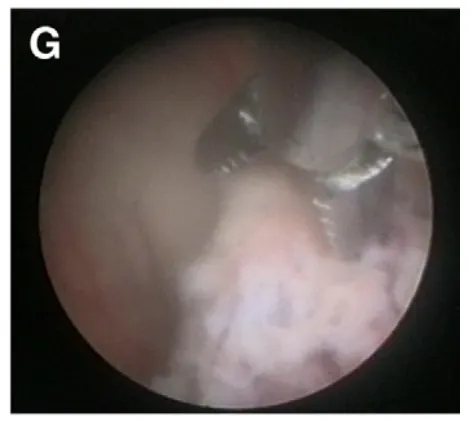
(G)使用抓钳切除肿瘤;
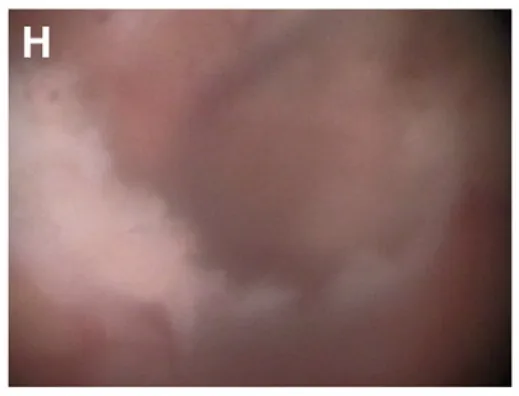
(H)肿瘤切除后可见透明隔的自由边缘。
施罗德教授的手术技术经验分享
通过脑室系统,内镜能够轻松抵达这些病变部位。此外,由于脑室内肿瘤常导致脑脊液(CSF)通路梗阻,进而引发脑室扩张,为内镜操作提供了充足的空间。
即使是脑室较为狭窄的患者,借助神经导航技术也可精准、安全地到达病变部位。内镜在脑室内肿瘤治疗中的目标通常包括:解除脑脊液通路梗阻、明确组织学诊断,在可能的情况下力求完全切除肿瘤。
与显微外科切除相比,内镜入路的优势在于能够更好地照亮并清晰显示脑室深处的结构,同时减少对脑组织的分离和牵拉。由于内镜可通过简单钻孔插入,因此能够避免开颅手术。在经神经内镜手术中,内镜鞘的操作可有效保护周边重要结构,如胼胝体、下丘脑和血管等。
PART 01 复杂精密的手术设备系统
在神经内镜手术中,需要一套复杂且精密的设备系统。为了能够完全切除脑室内病变,必须具备较大的工作通道和有效的手术器械。如果使用小型抓钳和狭窄的工作通道,将很难实现有效的组织切除。
LOTTA 脑室镜的重要临床意义
脑室镜(Ventriculoscopy)是一种神经外科技术,主要用于脑室内疾病的诊断和治疗。该技术允许医生在脑室内进行可视化操作,以便对脑室内的病变进行评估和处理。脑室镜技术通常通过小切口进入,利用其照明和成像系统,为医生提供清晰的视野,从而实现精确操作。在神经外科领域,脑室镜技术具有重要的应用价值,尤其在处理脑室内的肿瘤、出血、感染等问题时,可通过较小的创伤实现诊断和治疗目的。
LOTTA 脑室镜具备极高的透光性能,即使在蛋白质丰富或混有血液的脑脊液中,也能呈现卓越的图像质量并保持安全的空间定向。其自带的 HOPKINS 柱状透镜拥有 6° 视角,极大地缩减了视觉盲区,如同为神经外科医生打开了大脑的 "房门",能够清晰观察到每个角落,成为医生们的一双 "慧眼"。
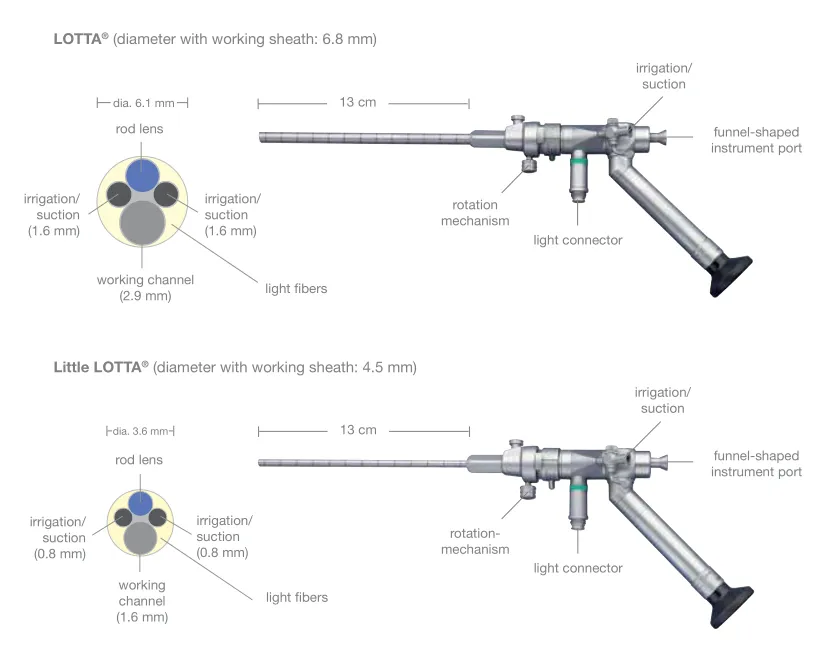
作为一种全方位解决方案,LOTTA 系统提供了灵活的选择:Little LOTTA 直径较小,操作更为便捷,适用于多种手术,如脑室造瘘术、隔膜造瘘术、肿瘤活检以及囊肿开窗术等;而标准 LOTTA 尺寸更大,除上述适应症外,还特别适用于胶样囊肿切除、肿瘤切除、支架植入术以及导水管成形术(伴或不伴后续支架置入)。
该系统由施罗德教授发明,并由国际知名内镜生产企业 KARL STORZ 生产。
PART 02 "干燥视野" 技术与止血注意事项
在止血方面,主要使用双极电凝探针或镊子。激光也可以作为替代工具,但激光设备成本较为高昂。由于在内镜肿瘤切除过程中出血较为常见,因此需要持续打水以保持视野清晰。理想的设备是电动流量和压力控制泵。
在需要短时间强力灌注时,可以使用注射器。乳酸林格氏液(温度控制在 36℃–37℃)是首选,因为与大量生理盐水灌注后常见的术后体温升高相比,使用乳酸林格氏液后很少出现这种情况。为了避免颅内压(ICP)危险性升高,必须确保灌注液有足够的流出通道。在出血情况下,切勿拔出内镜,而应保持其原位,进行冲洗并等待。
在肿瘤分离过程中,对于可能受损的较大血管,应在出血发生之前使用双极电凝进行烧灼处理。在极少数严重出血的情况下,需要抽吸脑脊液(CSF)以获得干燥的手术视野。采用这种 "干燥视野" 技术,更容易识别出血血管,并能迅速实现止血。
神经内镜手术原则与术后管理要点
内镜治疗脑内和脑旁肿瘤的总体原则是先阻断肿瘤的血液供应,随后进行肿瘤减容。一般来说,采用分块切除的方式;然而,在某些肿瘤中,可以将病变从周围脑组织中分离并完整切除。切除后,仔细止血至关重要,以避免再次出血。
在肿瘤切除后,需要检查切除部位以确保没有活动性出血。同时,对脑室进行彻底冲洗以清除血块。通常情况下,不放置外部脑室引流管。施罗德教授会用明胶海绵填塞颅骨钻孔,并紧密缝合帽状腱膜,以防止帽状腱膜下脑脊液积聚和瘘管形成。皮肤则用连续无创缝线缝合。一般来说,患者会在 ICU 观察一晚。

 胶质瘤
胶质瘤 垂体瘤
垂体瘤 脑膜瘤
脑膜瘤 脑血管瘤
脑血管瘤 听神经瘤
听神经瘤 脊索瘤
脊索瘤




 沪公网安备31010902002694号
沪公网安备31010902002694号