自首项随机临床试验证实颞叶切除术对难治性颞叶癫痫的疗效优于药物治疗以来,癫痫外科手术领域已发生显著变革。外科手术目前仍是难治性癫痫的主要干预手段,尽管其发展趋势已从大型开放式手术逐渐转向微创、神经调控、靶向性离断或消融手术。
这一转变主要由神经外科医生、神经科医生、神经生理学家、工程师及基础科学家等多学科专家的共同努力所推动,得益于近期的技术进步。现代癫痫外科医生正越来越多地采用技术辅助手段,这些手段不仅影响着手术决策流程,也改变了通过外科手术定位致痫区的方式。机器人应用、激光技术、无线记录、术中成像、新型神经调控技术以及高强度聚焦超声仅是其中几个例证,它们凸显了癫痫手术为何正变得更具吸引力。这些进展在两年一度的“癫痫手术技术会议”上得到了广泛探讨。理想情况下,这将有助于缩短患者转诊至专业癫痫治疗计划的时间,并可能缩小手术治疗的可及性差距。
本篇综述源自INC旗下世界神经外科顾问团成员、世界神经外科学院前主席、国际神经外科知名杂志《Journal of Neurosurgery》主编、加拿大的James T. Rutka教授于2020年发表于癫痫领域期刊《Epilepsia》(影响因子:5.562)的论文。该文综述了机器人技术与SEEG立体定位脑电波电极置放术在癫痫手术中的应用及其面临的挑战。

在过去的2至3年间,通过颅骨切开术或钻孔将硬膜下电极(SDE)植入大脑,已成为北美、英国、德国及奥地利等地进行有创脑电图记录的主要方法。与之不同的是,蒙特利尔、法国及意大利的学术中心则倡导采用源自Talairach立体脑电图(即立体定位脑电波电极放置术,SEEG)方法的技术,通过旋转钻孔将深度电极置入脑内。这两种方式已共存近半个世纪。近期,深度电极刺激方法在许多中心悄然受到欢迎。立体定向机器人与3D导航平台的出现,在很大程度上推动了这一发展,促使传统的SDE方式向深部电极刺激方式转换。然而,SDE与深度电极技术各自具备的特定优点与缺点,仍需得到充分关注。
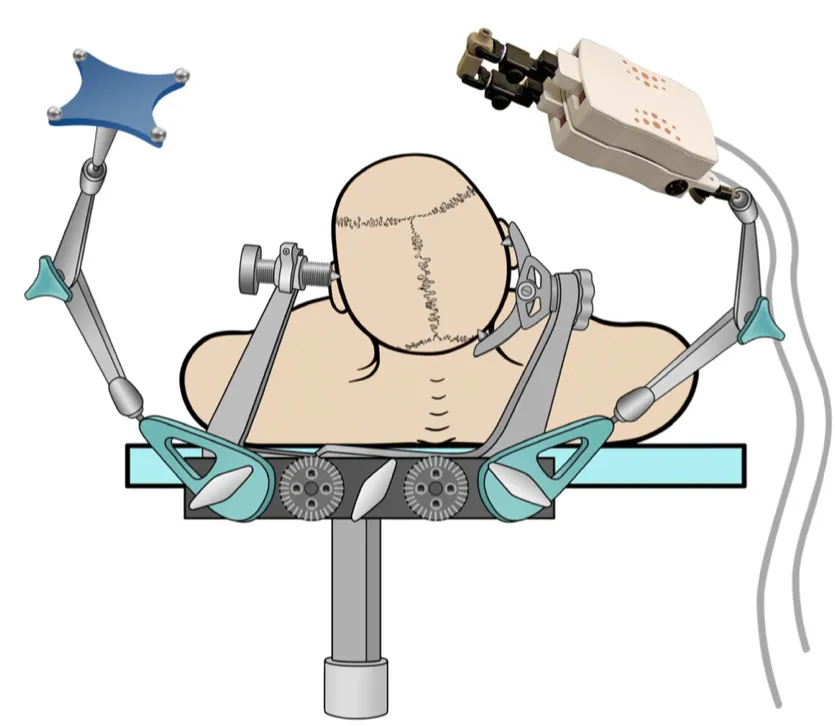
图1:在神经导航辅助下用于植入深度电极的微型机器人设备示意图。图中显示头部固定于标准头架中,配有导航参考架,机器人通过适配器连接。
可以从多个方面解释这种向SEEG方法过渡的成功。首先,有证据表明深部电极手术的并发症发生率及致病率低于SDE植入术。SDE植入术后报告的并发症发生率为5%至17%,而SEEG方式的并发症发生率则小于1%。其次,除了新的立体定向方法,放射学与计算技术的创新,以及大量导航图像引导应用的引入,使得电极植入过程更为便捷、快速。SEEG能够以更简化、高效且精确的方式实现更多目标。为满足这些需求,自动轨迹规划技术得以开发。第三,这些优势被转化为机器人应用,旨在进一步提升植入准确性并优化手术流程(见图1)。
目前临床中使用的机器人系统主要有3种,且各治疗中心之间的使用情况差异显著。这些差异体现在图像采集、轨迹规划、患者定位、头部固定、患者配准以及植入方法本身等多个环节。
所有这些步骤都可能影响整体工作流程、感知的准确性以及最终的手术结果。外科工作流程的差异部分源于操作者既往接受的培训类型、个人经验以及外科专业背景,而非完全由客观因素决定。若神经外科医生接受过立体定向神经外科的培训,则可能更倾向于在机器人辅助下使用立体定向框架。另一方面,不习惯立体定向手术的医生则可能更愿意使用头架。同样,若医生习惯于使用导航系统,则可能倾向于选择结合了神经导航功能的机器人,而非传统的立体定向技术。
机器人应用的支持者认为,与传统“手动”方法相比,机器人系统能提供更好的总体精度。
近期一项荟萃分析评估了13种不同的电极植入系统,包括无框架系统、基于框架的系统以及机器人系统。该研究表明,机器人系统的性能至少不逊于经典的基于框架的系统,并且优于无框架系统。
具体而言,机器人轨迹引导系统的进入点误差(EPE)为1.17毫米,目标点误差(TPE)为1.71毫米。相比之下,基于框架系统和无框架系统的EPE分别为1.43毫米和2.45毫米,TPE分别为1.93毫米和2.89毫米。然而,这些比较是基于回顾性的、使用基于框架和无框架系统的病例系列进行的。目前,在机器人轨迹引导系统与其他技术之间,或者在不同机器人轨迹引导系统自身之间,尚缺乏足够的前瞻性比较研究。但可以明确的是,机器人系统不太可能比现代基于框架的系统精度更低。尽管较少被讨论,但参考图像的选择和配准方法本身会极大地影响整体操作的准确性。事实证明,基于CT的框架配准是确定进入点的最精确方法,其EPE可小于1毫米;其次是CT激光配准,EPE小于2毫米;最后是磁共振成像(MRI)激光配准,其EPE约为3毫米。
因此,先前的研究还表明,基于基准标记的配准比基于表面轮廓的配准更精确,而基于CT的表面配准又比使用MRI的表面配准更精确。为了最大限度地减少辐射暴露(尤其是在儿科患者中),3T MRI已被证明适用于大多数立体定向手术。此外,新颖的3D计算机模型现在可以通过自动血管检测功能,进一步提高手术规划的准确性与安全性。
然而,仍然存在一个问题:这种追求更高精度的驱动力是否合理?以及在规划SEEG植入时,是否完全有必要达到与深部脑刺激(DBS)手术相提并论的精度水平?
如果答案是否定的,那么使用机器人应用程序的主要论据之一就会被相对弱化。
与DBS手术相比,深度电极植入的典型平均轨迹长度在4到5厘米之间,这大约是典型DBS轨迹长度的一半。
此外,深度电极的常用靶点(即植入位置)本身可能并非高度明确的结构。
深度电极植入所需的精度可能取决于轨迹规划的类型。例如,需要穿过脑沟回或外侧裂的轨迹,可能要求更高的植入精度。
在某些情况下,结合使用深度电极和硬膜下电极的方案,将需要不同的规划策略。
对于额叶、顶叶和枕叶的内侧皮质,可以通过植入半球间硬膜下电极配合更长的正交深度电极来实现监测。
这些概念上的差异影响了手术轨迹的长度,进而影响了所需的精度水平。
既往报道中深度电极植入的低并发症发生率,可能反映了这样一个事实:外科医生在规划轨迹时,能够很好地预测其应用方法的误差范围。
关于机器人应用的另一个争议点在于,它们是否能够减少总体手术时间以及植入每个电极所需的时间。
实际上,据报道,使用机器人应用植入每个电极的平均时间约为10分钟,这比使用人工神经导航技术报告的12-15分钟略快。
然而,这些报告通常没有考虑使用机器人应用程序所需进行的术前检查准备,以及手术室内的额外设置时间。
考虑到这些额外时间,所报告的手术时间节省可能会被部分抵消。
实际的手术操作时间可能不那么依赖于技术本身,而是取决于手术过程中涉及的团队协作与基础设施。
这些因素很难量化评估,并且依赖于国家政策、特定医疗机构的规章制度以及组织和行政流程。
在许多医疗中心,侵入性记录范式突然转向倾向于使用SEEG而非SDE,通常忽略了一个事实:当需要进行皮层功能测绘时,通常使用SDE可以更好地实现这一目标。
因此,每个癫痫中心都应同时提供SEEG和SDE技术,并且必须基于患者的具体情况选择最适当的技术。
此外,机器人系统价格昂贵,并且其主要用途通常仅限于SEEG电极植入。
该系统的投资回收期很长。尽管可以预期随着时间的推移硬件价格会下降,但有时仍无法实现预期的投资回报。
可以预见,某些机构目前不会开始购置该技术,尤其是当它们已经拥有一个完善的、基于框架的立体定向手术程序时。
参考资料:How technology is driving the landscape of epilepsy surgery. Epilepsia. 2020;00:115.

 胶质瘤
胶质瘤 垂体瘤
垂体瘤 脑膜瘤
脑膜瘤 脑血管瘤
脑血管瘤 听神经瘤
听神经瘤 脊索瘤
脊索瘤




 沪公网安备31010902002694号
沪公网安备31010902002694号