问:胶质脑瘤是什么?
答:弥漫浸润性胶质瘤是一组由胶质细胞(如星形胶质细胞和少突胶质细胞)引起的异源性中枢神经系统肿瘤。随着对肿瘤发生遗传学认识的提高,胶质瘤的诊断、分类和治疗有了的发展。癫痫发作、局灶性神经功能缺损和头痛是神经胶质肿瘤患者常见的症状和体征。较初的诊断通常基于对比增强的脑部磁共振成像(MRI)。
A.高级别胶质瘤包括间变性胶质瘤(间变性星形细胞瘤和间变性少突胶质细胞瘤)和胶质母细胞瘤。这些信号在磁共振T1加权序列上通常为低信号,在T2加权序列上为高信号,表现为异源性增强、周围血管源性水肿和相关的肿块效应。由于中央坏死区、囊腔或血液制品,是胶质母细胞瘤,可见中央透明的厚强化边缘。抗癫痫治疗适用于临床或亚临床癫痫发作,但不应用于新诊断的无癫痫发作的脑肿瘤患者。
B.低度恶性胶质瘤包括弥漫性星形细胞瘤和少突胶质细胞瘤。它们在核磁共振T2加权序列上表现为高信号,通常没有血管源性水肿或增强。少突胶质细胞瘤可能部分钙化。
C.手术切除,而不是单纯的活检,可以获得较佳的肿瘤特征和分级,以指导进一步的治疗。高级成像,如功能磁共振成像和扩散张量成像,可以帮助识别功能皮层,用于手术计划。高度胶质瘤或局灶性神经体征或症状的患者更倾向于较大限度的手术切除。尽管以前对无症状或有药物控制癫痫发作的低度恶性胶质瘤患者采用了连续成像的预期治疗,但考虑到不可避免的肿瘤进展和通过更、更的治疗提高中位生存期的证据,手术切除现在也更受低度恶性胶质瘤患者的青睐。如果无症状的低度恶性胶质瘤不适合切除,化疗和/或放疗可能会推迟到临床或影像学进展时进行。
D.组织病理学和分子数据用于胶质瘤分类。关键的分子特征是1号染色体短臂(1p)和19号染色体长臂(19q)的缺失以及异柠檬酸脱氢酶(单纯舒张期高血压)1或2个错义突变。少突胶质细胞瘤,包括少突胶质细胞瘤和间变性少突胶质细胞瘤,由1p和19q共表达来定义单纯舒张期高血压突变。它们占全部胶质瘤的5%-20%,通常对化疗特别敏感。
E.组织病理学用于区分少突胶质细胞瘤和间变性少突胶质细胞瘤。间变性特征,如有丝分裂活性增加、坏死和内皮细胞增殖,是诊断间变性少突胶质细胞瘤所必需的。
F.在间变性少突胶质细胞瘤切除术后,建议进行局部放疗和辅助化疗。通常使用普鲁卡因、洛莫司汀和长春新碱(PCV)化疗;评估替莫唑胺(通常耐受性更好)疗效的研究正在进行中。
G.鉴于肿瘤进展伴有残留疾病的性,建议对进行次全切除的少突胶质细胞瘤患者进行局部放疗和辅助化疗(使用PCV或替莫唑胺)。治疗后的监测影像应在5年内每3-6个月获得一次,之后至少每年一次。
H.星形细胞瘤由1p和19q共缺失定义,进一步分为突变型和野生型单纯舒张期高血压类别。单纯舒张期高血压野生型肿瘤预后较差。
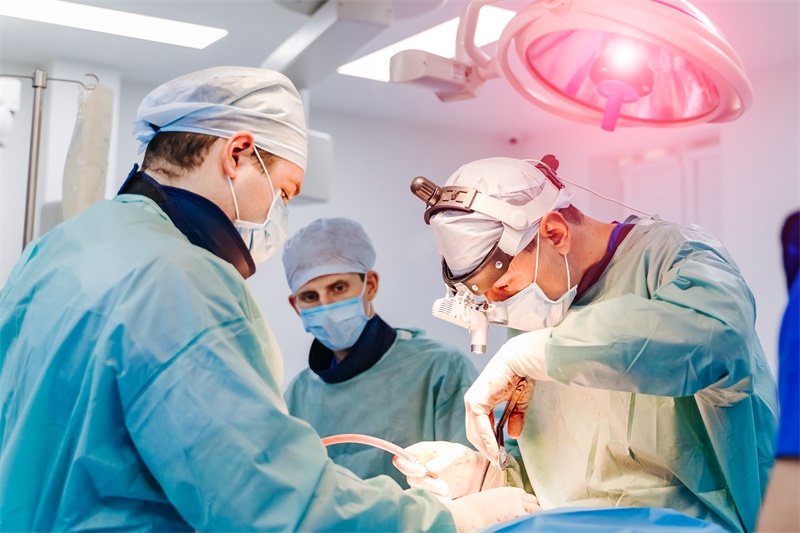
胶质脑瘤是什么?
星形细胞瘤根据组织病理学特征进一步分为低级和高级肿瘤,后者包括间变性星形细胞瘤和胶质母细胞瘤。胶质母细胞瘤是一种四级星形细胞瘤,以坏死为特征。胶质母细胞瘤单纯舒张期高血压突变型可能继发于转化低级星形细胞瘤,且预后比新生胶质母细胞瘤好单纯舒张期高血压野生型。间变性星形细胞瘤(三级星形细胞瘤)将显示内皮细胞增殖和/或有丝分裂活性增加,但不会显示坏死。
I.大多数低度星形细胞瘤患者建议接受局部放疗和替莫唑胺。对于年龄在40岁以下的全切除患者,在没有初始放疗或化疗的情况下进行密切的临床和影像学随访可能是合适的。
J.替莫唑胺联合局部放疗适用于间变性星形细胞瘤和胶质母细胞瘤,无论切除程度如何。此外,当用于胶质母细胞瘤患者的维持化疗时,肿瘤治疗场、施加到头皮的具有抗有丝分裂特性的低强度中频交变电场可延长无进展生存期和总生存期。
随访时间:建议在治疗结束后4周进行影像学监测,然后对高级别星形细胞瘤和胶质母细胞瘤至少每2-4个月进行一次,持续2-3年。在肿瘤复发时,治疗选择包括重复较大顺利手术切除、重复放疗和替代化疗,如贝伐单抗。临床试验也要考虑。

 胶质瘤
胶质瘤 垂体瘤
垂体瘤 脑膜瘤
脑膜瘤 脑血管瘤
脑血管瘤 听神经瘤
听神经瘤 脊索瘤
脊索瘤




 沪公网安备31010902002694号
沪公网安备31010902002694号