脑室内脑膜瘤属于相对罕见的颅内病变,当其发生时肿瘤体积通常较大,最常见发生部位为侧脑室前角区,左侧发生率略高于右侧。回顾20世纪80年代的相关研究系列,脑室内脑膜瘤相关并发症发生率较高,甚至存在一定死亡率,死亡原因多与术后脑室内出血密切相关。目前,此类肿瘤已可通过安全切除手术获得良好预后。
本文描述一种中线旁的经顶叶入路变式。该入路设计能够最大限度降低对该区域重要白质纤维束的损伤风险,允许肿瘤向内侧及外侧方向移动以便处理其供血血管,同时入路角度便于术者相对于关键解剖结构进行精确定位。
病例报告
一位54岁女性患者临床表现为数周间歇性头痛。术前检查实施磁共振平扫及增强扫描,采用1毫米层厚扫描数据用于三维神经导航重建。同时获取弥散张量成像数据,并在患者磁共振三维脑空间内重建白质纤维束。重建所得三维坐标文件用于术中神经导航系统。
磁共振成像检查结果显示一处强化的脑室内占位性病变。图1A-C为钆增强T1加权磁共振图像,清晰显示位于左侧侧脑室前角区边界清楚、明显强化的病灶。影响此类病变手术入路选择的因素众多,特别是该区域周围的白质通路分布。术前弥散张量成像可对该区域白质纤维束进行细致评估。图1D-I呈现该区域弥散张量白质纤维重建结果。虽然处理侧脑室前角区病变已有经颞叶入路的文献描述,但图1中的重建图像显示密集的弓状束和上纵束阻挡了经颞叶的手术通道。图1J-L底部区域为术后磁共振图像,显示通过中线旁经顶叶手术入路实现的肿瘤全切。
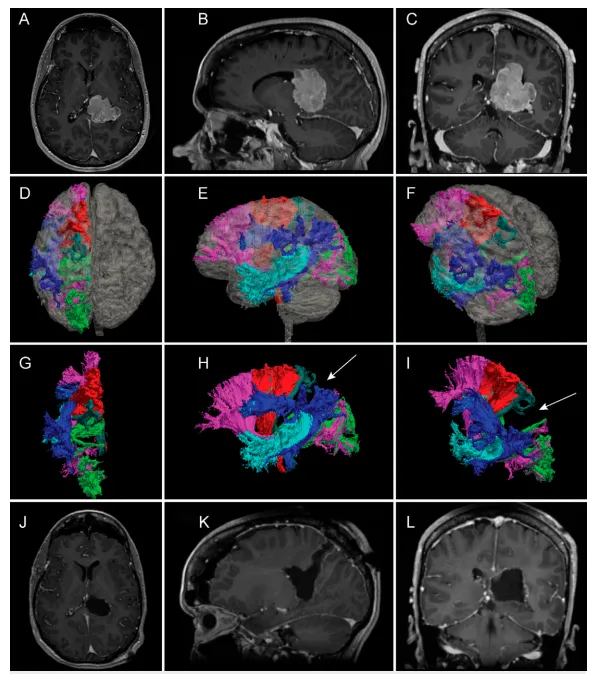
A–C:术前T1加权钆增强磁共振成像显示优势半球脑室内脑膜瘤的轴位、矢状位及冠状位图像。
D–I:弥散张量纤维束成像三维重建的主要白质纤维束。图D、E、F分别为叠加患者磁共振透明重建模型后的上视图、左侧视图及左上前斜视图。图G、H、I为不叠加磁共振脑图像时相同视角下的白质纤维束显示。各纤维束颜色标示如下:额枕下束呈粉红色;运动束呈红色;感觉束呈深绿色;视辐射呈黄绿色;上纵束呈深蓝色;弓状束呈浅蓝色。
J–L:显示患者经中线旁经顶叶入路实现全切后的术后磁共振影像。
经顶叶入路提供了避开重要白质纤维束的手术机会。先前研究文献描述的经顶叶入路多采用斜行轨迹。如图1D-I所示,经皮质、经顶叶的中线旁通道在前方以感觉束为界,后方以视辐射为界,下方以额枕束为界,外侧以上纵束和弓状束为界。图1中内侧区域无明显的重要白质纤维束分布,这表明从功能保护角度分析,中线旁轨迹可能属于最安全的手术路径。
为实现对肿瘤的中线旁入路,患者如图2所示取半躺卧位,收下颌,头部保持无旋转状态。该体位使手术轨迹与术者视线保持对齐。图2C图解了皮肤切口及开颅骨窗与矢状窦的解剖关系。在中线旁入路手术中,保护矢状窦这一重要的内侧结构至关重要。除静脉窦本身外,还应考虑并避免损伤流入矢状窦的大型静脉。术前可采用增强T1磁共振或静脉造影技术研究静脉解剖结构。
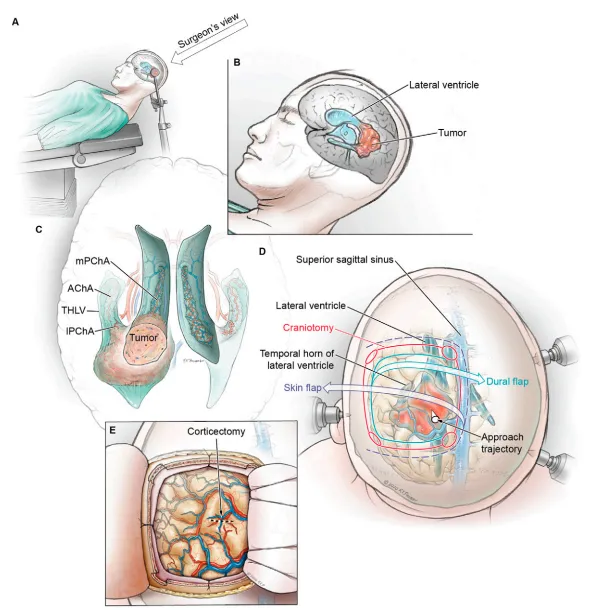
A:患者取仰卧半躺卧位,下颌微收。
B:头部定位及肿瘤在侧脑室前角位置的特写。
C:脑室系统内肿瘤示意图。
D:术者视角下的开颅术野,显示皮肤切口、开骨窗及硬膜切开范围与深部肿瘤的解剖关系。肿瘤位于透明皮质下方、矢状窦旁的脑室系统内。
E:骨瓣移除后术野,显示硬膜向内侧翻开、大脑皮质暴露。
AChA = 脉络膜前动脉;lPChA = 脉络膜后外侧动脉;mPChA = 脉络膜后内侧动脉;THLV = 侧脑室颞角。
采用如图2D所示的紧邻中线的倒U形皮肤切口。在靠近但不跨越中线的开颅骨窗的每个角部实施钻孔。其中最重要的钻孔位置为最靠近中线的两个骨孔,它们允许在靠近上矢状窦的这一关键内侧部分,将硬脑膜与骨瓣进行安全分离。在仔细分离和适当注意下,可安全地翻开骨瓣。
硬脑膜以C形方式切开,并向上矢状窦方向翻开。图2E显示了垂直于矢状窦进行的皮层切开操作。回顾图1H和I中白色箭头所示的轨迹,此入路成功避开了该区域的白质纤维束,直接通向肿瘤位置。为引导术者准确到达前角区的肿瘤,神经导航系统属于有用的辅助工具,特别是在矢状面定位方面。仔细的体位摆放可使术者准备一条非常直接、直视的手术轨迹。在内外侧平面上,保持患者头部无倾斜有助于获得一条平行于大脑镰和半球间裂由浅入深走行的解剖轨迹。测量轨迹深度同样有助于术者判断何时到达脑室腔隙。
图3描绘了逐步切除肿瘤的手术过程。前角区脑膜瘤的血液供应通常来源于脉络膜前动脉和脉络膜后动脉的分支血管。进入脑室时,这些血管最初不可直接观察。如图3A和B所示,必须首先对肿瘤进行内部减瘤操作,本病例中使用了超声吸引器设备。一旦肿瘤被有效掏空,即可移动肿瘤包膜以处理其供血血管,如图3C-F所示。
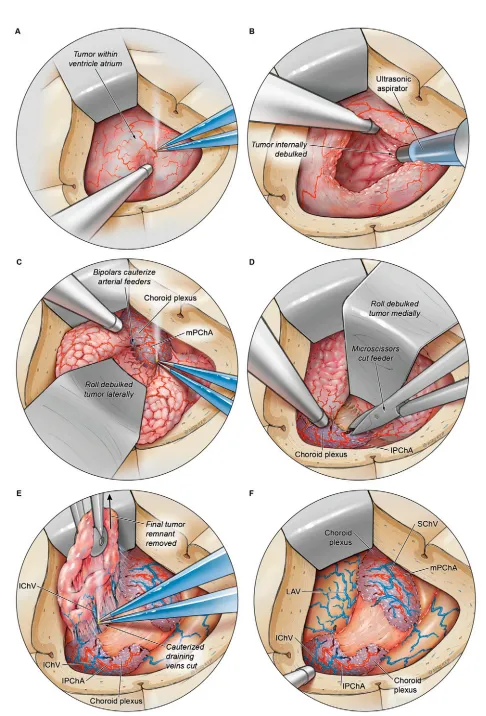
A、B:肿瘤切除步骤示意图,分别为初始显露肿瘤及初步减瘤。
C、D:向外侧移动肿瘤以处理内侧脉络膜后动脉供血支,向内侧移动肿瘤以处理外侧脉络膜后动脉供血支。
D、E:减瘤后肿瘤移除前,处理剩余引流血管蒂。
F:肿瘤切除后侧脑室前角区残腔。
AChA = 脉络膜前动脉;lPChA = 脉络膜后外侧动脉;LAV = 房外侧静脉;mPChA = 脉络膜后内侧动脉;SChV = 脉络膜上静脉。
将肿瘤向外侧方向翻转,以显露深部内侧包膜上的任何脉络膜供血血管。使用双极电凝镊电凝这些血管,并用显微剪刀切断,以游离肿瘤包膜便于进一步移动。随后,将肿瘤向内侧方向翻转,以处理包膜的前外侧下部区域,即脉络膜前动脉分支进入的部位。一旦这些血管以及肿瘤的引流静脉被充分电凝并切断,肿瘤应可自由移动。然后可在脑室内对肿瘤进行分块切除。最后以水密方式缝合硬脑膜。图1J-L的术后磁共振图像显示肿瘤实现全切。患者术后未出现神经功能缺损,最终于术后第3天出院回家。
经验总结
总之,前角区肿瘤的血管分布、功能影响和解剖学因素使其成为一种独特的神经外科疾病实体,需要术者进行仔细手术规划。对此入路存在两个合理的批评观点:一是相对较长的经皮质手术通道可能限制手术野的到达范围;二是处理供血血管的时间相对较晚。我们通过使用长柄超声吸引器和手术显微镜来解决前者问题。正确的患者体位摆放也可抵消深部手术通道伴随的操作困难。在肿瘤减瘤过程中,可使用牵开器谨慎地抬起皮层的上部,这部分皮层会开始坠入手术野。应注意避免实施过度牵拉操作,因为这也可能损伤附近的白质纤维束。
本文描述的入路方式,提供了一种有效的方法来处理该区域的肿瘤,在最大化肿瘤切除程度的同时,最小化手术致残风险。

案例来源:INC国际神经外科医生集团旗下组织世界神经外科顾问团(WANG)成员Mitchel S. Berger教授发表研究《Paramedian transparietal approach to a dominant hemisphere intraventricular meningioma: illustrative case》。


 胶质瘤
胶质瘤 垂体瘤
垂体瘤 脑膜瘤
脑膜瘤 脑血管瘤
脑血管瘤 听神经瘤
听神经瘤 脊索瘤
脊索瘤




 沪公网安备31010902002694号
沪公网安备31010902002694号