在过去的十年里,FDA批准了越来越多的针对实体瘤的免疫疗法,肿瘤包括黑色素瘤、肺癌、乳腺癌、腺癌、膀胱癌和肾癌(肾细胞)。许多这些批准预示着检查点封锁疗法(程序性死亡抗体1 [PD-1]和/或细胞毒性t淋巴细胞相关蛋白[CTLA-4]),这已经完全改变了我们对晚期甚至转移性癌症治疗的期望和能力。然而,胶质母细胞瘤(GBM)仍然是一个突出的抵抗。那么,GBM似乎只是免疫治疗阶段的后来者,然而,事实正好相反。
免疫疗法原理
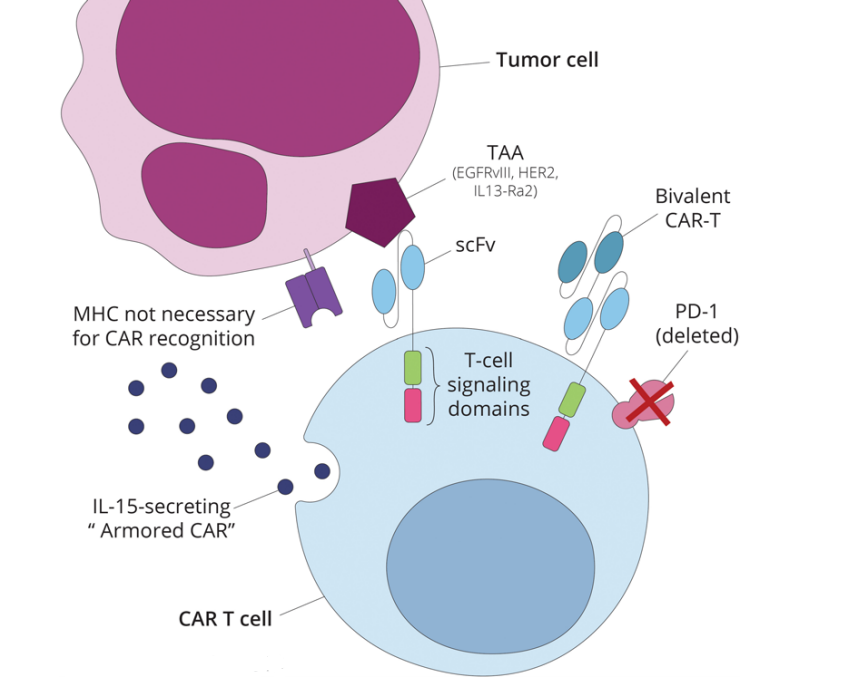
恶性神经胶质瘤免疫治疗
CAR-t细胞疗法。转染CAR-T细胞能够以mhc不依赖的方式识别肿瘤细胞表面抗原,从而诱导肿瘤细胞杀伤。
早在20世纪70年代初,布鲁克斯和罗兹曼等先锋者就研究了GBM与免疫系统的相互作用。同样,目前各种免疫治疗方法的一些较早的前身在20世纪80年代以GBM为目标进行了试验。之后,重点开始转向识别合适的抗原作为靶向。目前鉴定的胶质细胞相关抗原包括IL13Ra2、HER2、gp100、TRP2、EphA2、survivin、WT1、SOX2、SOX11、MAGE-A1、MAGE-A3、AIM2、SART1和巨细胞病毒(CMV)蛋白。表皮生长因子受体型(EGFRvIII)和IDH-1突变体(R132H)是的肿瘤特异性靶点。GBM和其他癌症的免疫治疗模式现在遍及各个领域,从抗体到过继细胞转移到疫苗,再到基于病毒的治疗,再到免疫检查点封锁。
需要指出的是,GBM给免疫治疗的成功带来了一系列独特的障碍。这归因于GBM的障碍包括:肿瘤突变负担低;广泛的肿瘤异质性;受限的中枢神经系统药物/免疫通路,也许更为的原因是t细胞功能障碍。神外专家们还需关注两个特别突出的免疫学问题:免疫获取和免疫控制。脑瘤患者也需要明确——在免疫治疗这一领域还有很多问题亟待解决。
预防GBM的免疫治疗效果有限
尽管经过几十年的努力,预防GBM的免疫治疗效果有限。肿瘤及其中枢神经系统的局限性同样给免疫治疗带来了独特的挑战,包括药物和免疫通路的限制,的异质性,低突变负担,以及严重的肿瘤引起的t细胞和其他免疫功能障碍。还有一些新发现的难题,如骨髓中T细胞的肿瘤定向隔离,让神外专家们意识到他们仍需阐明大脑限制免疫反应的复杂机制。尽管失败了,我们继续更好地了解这些局限性,并相应地调整我们的治疗策略。新辅助检查点封锁试验的较新结果为我们解码治疗耐药性的机制提供了新的乐观理由。重新关注预防和逆转t细胞功能障碍是必要的努力,将我们的治疗导入可行的和功能正常的免疫系统。
即使免疫治疗已经在取得一些好的成果,但目前恶性胶质瘤的一线治疗手段仍是手术切除,当然,尽可能切除肿瘤、术后辅助放化疗的综合治疗方案也是被广泛应用的,在综合治疗领域,INC旗下国际神经外科顾问团(WANG)的专家成员、国际神经外科学院前主席、儿童神经外科教授James T. Rutka教授具心得,作为加拿大多伦多大学儿童病院脑肿瘤研究中心主席,Rutka教授带领的团队及Sickkid医院在小儿脑肿瘤手术和疾病研究方面在国际上都享有盛誉。2016年,他因在儿科脑肿瘤治疗和国际领导方面的成就而荣获加拿大更佳医生称号。国内患者如追求更好的治疗和预后效果,可拨打400-029-0925咨询INC国际专家远程咨询,还可以与Rutka教授“面对面”沟通病情,提出问题后,教授会为患者定制专属综合治疗方案。
参考文献:Doi:10.3171 / 2019.5.JNS181762

 胶质瘤
胶质瘤 垂体瘤
垂体瘤 脑膜瘤
脑膜瘤 脑血管瘤
脑血管瘤 听神经瘤
听神经瘤 脊索瘤
脊索瘤




 沪公网安备31010902002694号
沪公网安备31010902002694号