听神经瘤的手术已经从一个死亡风险很高的阶段发展到追求切除肿瘤的同时保留听力和面神经功能。听神经瘤常伴听力下降和耳鸣,但随着MRI的广泛应用使得早期发现小肿瘤(小于2cm)成为可能,因此越来越多的患者可以表现为听力接近正常或具有实用听力。小肿瘤的较佳治疗方案仍有争议、值得继续研究,治疗方案包括观察等待(watchful waiting,WW)、SRS和显微外科切除(microsurgical resection,MS)。
神经外科医师协会(Congress of Neurological Surgeons,CNS)发布的“散发性听神经瘤患者听力保留指南”提出了患者咨询治疗方案时的一些不同建议,但并未应该选择哪一种方案,突出强调患者自己选择。基于指南的系统性综述比较了上述三种治疗方案随访2年、5年和10年后听力保留状况。
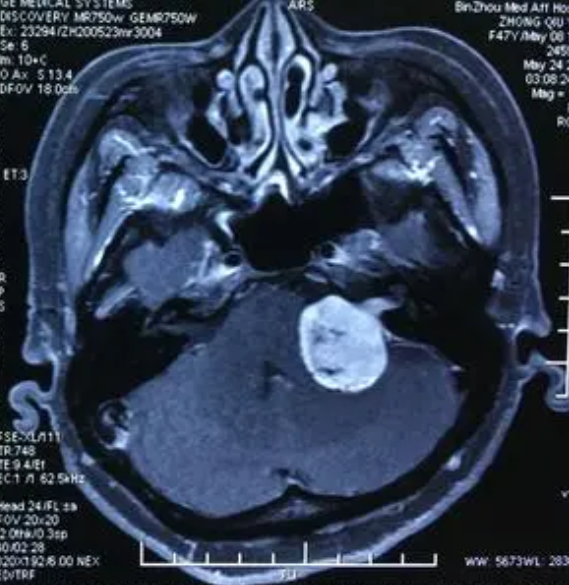
听力保留
后颅窝入路或乙状窦后入路尝试保留听力手术适用于肿瘤直径<1.5cm、术前听力良好者。Golfinos等比较了399例中小型听神经瘤(<28cm)接受手术和立体定向放射治疗的结果:SRS保留听力更好并发症更少,而面神经功能保留均好。综上所述,尽管SRS肿瘤控制率、听功能和面神经功能保留均好(是在小型听神经瘤),但并未根治肿瘤。如果这种保守治疗失败,由于接受过放射治疗导致再次手术时神经功能保留效果不尽人意。
单纯考虑听力保留、观察等待和SRS等无创方案表面具有的优势如果从长远来看也可能存在具体问题。实际上,随访观察中即使肿瘤未增大也会出现听力下降17.8;另一方面,系统综述报道放疗后短期内听力维持不变,但中远期可发生进行性、重度听力下降1127,9.10]。这些后遗症的数量并不比听力保留手术少”,因此,术前具有实用听力者应尝试保留听力手术”。
现有听力保留手术相关文献在选择理想患者、具体手术技术和平均随访时间等方面缺乏统一标准。Mazzoni等报道了1976-2009年322例听力保留手术资料,但不同时期入组标准各异,作者较后提出的标准是术前AAO-HNS分级A级、肿瘤≤10mm、ABR正常。通过回顾分析发现共有42例符合这个标准,其中,48%保留了A级听力83%保留了实用性听力。作者根据PTA和SDS对上述42例患者的队列进一步分层:发现术前PTA<20dB、SDS≥80%者76%术后保持AAO-HNSA级听力。由此可见,肿瘤大小和术前听力状态是术后短期听力良好的较重要评估指标。根据影像学观察,肿瘤引致内听道扩大也有判断预后价值。CT骨窗显示内听道直径越大,说明肿瘤压迫耳蜗神经越重,术后听觉功能丧失可能性越大。
Yang 等研究乙状窦后人路听觉功能保留情况12):回顾性分析了肿瘤小于20mm、听力为AAO-HNSA~D级这组患者的资料。36%术前具有实用性听力者(与Mazzoni相比例数和分组更多1)其听力得以保留;如果根据肿瘤大小分组后再分析,则听力保留者增加到48%,听神经瘤≤10mm 明显好于大肿瘤(P<005)。此外,Yang等认为术前高频听阈阈值评估术后PTA比术前低频听阈阈值和ABR的价值更大12),特别是ABR与术后听力无关。2006年Samii等报道 200例接受乙状窦后人路者全切率达大概率,51%保留了听力3。他们认为小听神经瘤(直径<20mm)可以达到全切且一期治愈并可保留神经功能,术前具有实用听力者可以保留听力。
大型听神经瘤手术听力保留效果存在争议,取决于如何定义大型标准。Wanibuchi等报道592例>2cm者听力保留率为53.7%[14)。Di Maio 等报道28例≥3cm 者听力保留率为21.4%15,术前AAO-HNS A类患者听力保留率达到30.8%。虽然肿瘤大小与较终听力保留结果呈负相关,但现有证据强烈提示术前听力与术后听力密切相关,即使那些不严格的队列研究中也是如此。此外,DiMaio等提出两个独自预后良好指标5,术前MRI显示内听道底部存在脑脊液;IAC纵轴前方肿瘤体积/肿瘤总体积比值<35%。
术后短期听力常用于评估外科医师保留耳蜗神经解剖结构的能力但即使在耳蜗神经完整保留者也有报道出现术后即刻全聋或听力下降。此时需考虑耳蜗本身对诱发和传递电脉冲的作用。事实上,可能发生毛细胞功能丧失,合理的解释是在手术时暴露和损伤了供应经的内听动脉,而听神经受损时完整保留内听动脉较其困难。也有很多更复杂的病例报道,术后成功保留听力但长期随访发现听力衰退11,17.18)。Strauss 等提出手术操作可能导致神经内膜滋养血管的微循环失调9。在神经缺血期间和缺血之后微循环失调可导致释放大量谷氨酸,转而导致钙离子流入受损神经元造成细胞死亡。切除肿瘤所致机械性或微血管损伤较初可能只影响耳蜗神经远端部分(反映为ABR的I波之外其他波出现延迟)然后随着神经变性的进展I波逐渐消失。
较近Ahsan等对优选手术者远期听力结果进行Meta分析显示如果术后早期保留了实用听力,5年内较有可能保住听力。术后即刻保听率为50%~70%,远期平均听力保留率为70%,35%~49%接受保听手术者在术后5年内将继续保持实用听力(AAO-HNSA级或B级)。上述数据与接受保守治疗的听神经瘤患者长期听力保留水平一致,后者范围在41%~57%之间。同时,据报道立体定向放疗后3年和10年的听力保留率分别为74%和44.5%8。Ahsan等还报道那些术后早期随访SDS≥89%者远期听力保留效果更好,这说明即使听力正常的听神经瘤患者优选手术也是合理的。Meta分析证实只有术前和术后PTA结果与长期听力保留有关,这种关系也经Nakamizo等证实。
后来有作者分析经乙状窦后人路治疗单侧听神经瘤患者平均随访5年的远期听力结果,7例患者术后6个月内复查PTA,发现其中2例患者与术后即刻PTA相比其PTA听阈降低≥5dB,末次随访时PTA听阈降低≥15dB;其余5例患者术后6个月复查时PTA下降<5dB,较终随访时PTA下降<15dB(P=0.04)。因此,术后早期 PTA听阈降低可能有助于评估听功能的远期预后。Mazzoni等甚至进行了6年以上时间(6~21年)的更长随访,他们发现87%术后早期听力正常者在长期随访结束时听力保持不变这意味着13%的患者出现了听力减退,与此前一些作者的研究结果完全一致四。从范围来看,189例术前为AAO-HNSA级或B级的患者中54例术后短期保了听,47例术后长期保住了听力,短期和长期保听率分别高达29%和25%。虽然效果良好,但作者认为此结果并不优于立体定向放射治疗的长期效果。但值得注意的是,与后来类似的研究相比,本研究中听力保留手术采用的标准不一致且更不严谨叫,因此,预期长期随访结果应该更好。
术中耳蜗神经监测
根据CNS较新指南20),术前具有可测听力、肿瘤直径<1.5cm的听神经瘤患者尝试听力保留手术时应使用术中耳蜗神经监测( intraoperative cochlear nerve monitoring,IOCNM)。至于较佳IOCNM技术,目前尚无足够证据表明直接监测听神经优于远场ABRs(20]ABR是一种需要专用设备的远场诱发电位,全麻后在外耳道内放置一个带12英寸塑料管的软耳模并予以密封,表面电较放置在头顶(Cz)和两侧耳垂(A1和A2)利用双通道(A1-Cz和A2-Cz)引出和收集健侧反应122)。向患侧发出31~51Hz、90~100dB声压的短咔嗒声或音调声,利用50dB白噪声掩蔽健耳21,22],术前记录两耳基线反应作为整个手术过程监测的基线。典型ABR包括5~7个峰,均在给声后10ms内产生,临床上前5个峰(波I~V)较重要。V波和V波产生于上脑桥和中脑下部。波V往往较粗大,手术期间需要密切监测。 V波潜伏期延长超过05ms或任何波形变化消失时应提醒外科医师(23]。 ABR的主要缺点是反应波幅小于lμV,因此需要叠加和长时间采集数据才能获得足够的信噪比。因此,ABR技术的瞬时分辨率较差,且易受术中各种因素干扰,包括切开硬膜、盐水冲洗术野、手术显微镜、高速电钻、超声吸引器等。尽管如此,2016年Hummel 等报道ABR可以作为评估术后耳蜗神经功能的指标[24]60%的病例显示肿瘤切除后 ABR 波形质量评估听结果的独自指标,BR受到影响可能是切除肿瘤过程中对耳蜗神经的进行性损害,也可能是手术较后阶段从耳蜗神经表面剥离肿瘤包膜时损伤神经。
经典ABR的较新进展是CE-Chirp*ABR,这是一种应用于新生儿听力检测的新型声刺激,旨在增强神经同步性、更快地检测出大波幅V波。Claus Elberling开发的CE-Chirp声刺激与常用的方波短声刺激具有相同的频谱和标准,CE-Chirp刺激产生的声能几乎同时到达耳蜗的全部区域[25,26。它们的区别在于声音刺激的低、中、高频成分的呈现时间不同,这种变化抵消了耳蜗行波力学作用。导致ABR波幅增加超过正常听力者相应短声引出的ABR波形25.25。
Mastronardi等初步研究发现在全部患者中经典的ABR需要大约1000个刺激才能引出一个清晰、可监测的V波22],而使用CE- ChirpABR只需要大约600个刺激即可,从而减少了成功刺激所需时间。此外,每次扫描的分析时间为10s,这使得监测小组能够在V波变化或消失时及时提醒外科医师。上述作者进一步研究患者术后听力保留效果,以肿瘤大小为参照,术中使用水平特异性(LS)-CE- Chirp*ABR监测。选取25例术前AAO-HNS分级为A、B级听力的患者,根据肿瘤大小分为A组(2cm)和B组(>2cm),总保听率为52%,其中组为61.5%,B组为41.7%(P-0014)两组之间有性差异。
Yamakami 等在乙状窦后入路切除小听神经瘤时使用了一种新设计的颅内电较对耳蜗神经复合动作电位(cochlear nerve compound action potentials,CNAPs)进行连续监测27。CNAP是一种近场诱发电位,颅内电较直接放置于脑池段耳蜗神经上,这种电较将一小簇棉花固定在一根细致、可延展、包裹乌拉坦的导线。根据他们的研究报道,切开硬膜后尽快识别脑池段耳蜗神经[27),将颅内电较置于脑桥小脑角肿瘤内侧靠近脑桥耳蜗神经根部,然后用小棉片包裹固定,将电较与术野隔开。放好电较后、开始切除肿瘤前记录基线CAP,整个硬膜内手术过程中持续监测CNAPs。
CNAP单个耳蜗神经纤维信号的总和。肿瘤压迫耳蜗神经导致单个神经纤维传导阻滞、电信号去同步化,去同步化本身导致振幅下降甚至CNAPs消失。耳蜗神经减压可以缓解去同步化导致肿瘤切除后的反应幅度增加,因此,显微外科手术可导致CNAPs形态和强度发生动态变化。Yamakami等报道44例≤1.5cm的听神经瘤患者中72%术后具有实用听力[27-29]并得出结论,CNAP比经典ABR(方波短声刺激诱发)提供的监测结果更可靠(66%vs.32%,P<001)[27-29],保听概率更高29]。然而,Mastronardi等在直径≤2cm的听神经瘤手术中只有61.5%的保听率,似乎差别不大。这可能说明,尽管CNAP比传统ABR具有诸多优势,但CE-ChirpABR没有CNAP电较移位的风险,有待进一步研究直接比较两种技术。

 胶质瘤
胶质瘤 垂体瘤
垂体瘤 脑膜瘤
脑膜瘤 脑血管瘤
脑血管瘤 听神经瘤
听神经瘤 脊索瘤
脊索瘤




 沪公网安备31010902002694号
沪公网安备31010902002694号