选择要眼睛还是要孩子?
怀孕7个月时,突然看不见了,就医查出垂体瘤。虽然是良性的,但是医生回复让我完全崩溃——等孩子足月生产、但是可能视力会远远失去或者直接做手术,但是孩子可能保不住。让对于一个等待了7个月的准妈妈太残酷……虽然在保护孩子的情况下,也切除了肿瘤,然而术后1年复发了,究其原因,可能是没切干净。
垂体瘤复发后选择放疗,还能不能生孩子呀?
无功能垂体瘤一开始切干净了,一年后就复发了。二次手术残留了,现在医生建议放疗。但是我还有生育需求,放疗后还能正常怀孕生子吗?复发后究竟该如何治疗?
INC福教授垂体瘤部分案例
(点击文章标题可跳转阅读患者案例详情)
◉垂体瘤手术+放疗后仍继续生长侵袭海绵窦,INC福教授不开颅手术后3年没有复发!
◉较大垂体瘤耐药又术后复发、面临失明,还能再手术、拯救视力吗?
◉垂体瘤经鼻内镜手术就是微创?INC两大国际教授:我们怎么做?
◉国际提出者“筷子技术”神经内镜手术教授福洛里希脊索瘤/垂体瘤全切除案例
1. 良性垂体瘤,为什么还让他们如此惊慌害怕?
垂体腺瘤是良性的,在大多数患者中生长缓慢的肿瘤,每年临床相关肿瘤的发病率为4 - 7 / 10万。手术通常是对对视觉通路有压迫的较大的无功能性腺瘤和除泌乳素瘤以外大多数功能性肿瘤的一线治疗。由于解剖学的限制,一开始手术时如果不能完全切除,在这些患者中,进展或复发往往是不可避免的。不完全切除有很高的复发率,这取决于残留病变的体积。此外,还会带来激素分泌超量的一系列问题。
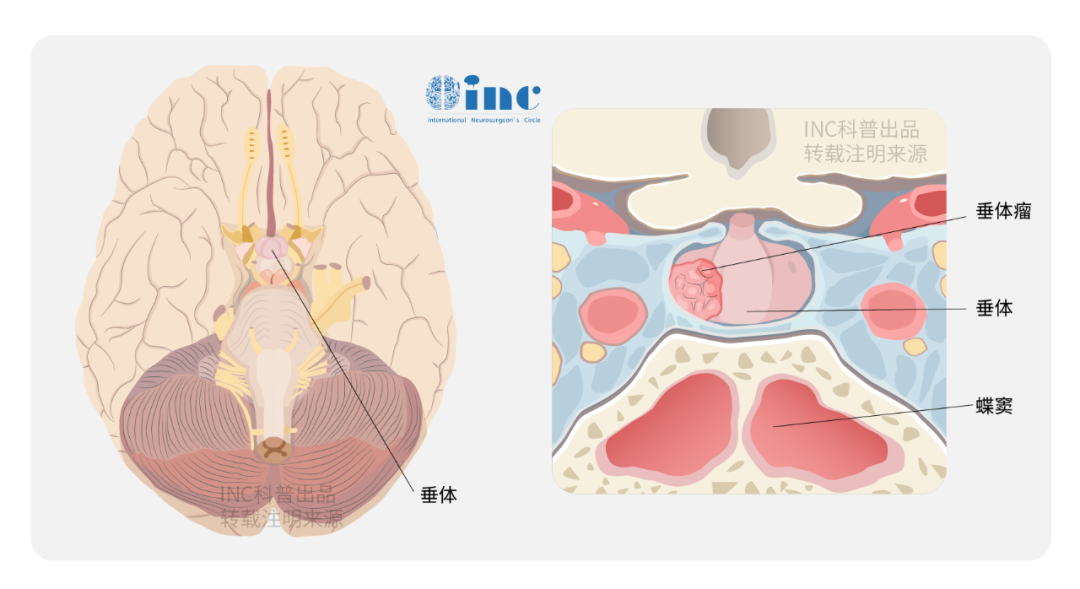
各种类型的垂体大腺瘤可压迫、浸润垂体及其周围组织,引发垂体前叶激素分泌不足导致垂体前叶功能减退;压迫视神经、视交叉,引起视野缺损和视力减退;若肿瘤向两侧生长,可包绕海绵窦,影响Ⅲ、Ⅳ、Ⅵ对颅神经及Ⅴ对颅神经眼支功能,引起眼睑下垂、瞳孔对光反射消失、复视、眼球运动障碍及面部疼痛等海绵窦综合征表现;垂体较大腺瘤可出现头痛、恶心、呕吐和颅压增高表现。部分垂体腺瘤可出现垂体卒中。
2. 垂体瘤复发VS再生长一样吗?
肿瘤复发和再生长有何不同?
肿瘤是否复发?
多数患者的肿瘤完全切除后不再复发,但仍有个别病例肿瘤再生长,生长的部位一般在原来肿瘤部位。一般术后一年复查1-2次,若无临床症状及影像学异常,复查次数逐渐减少。
肿瘤是否再生长?
严格来讲,肿瘤复发与肿瘤再生长定义不同,前者指手术将肿瘤已完全切除,以后颅内又生长同类肿瘤;后者系指手术将肿瘤部分切除,颅内仍残留一部分,以后残瘤再生长。这种情况复查次数较前者为多,因病情各异,复查次数、间隔时间根据具体情况而定,出现临床不适症状或原有症状加重应及时复查。经过复查及时发现问题,给予及时治疗。
3. 垂体瘤为什么易复发?
垂体术后5 - 10年复发的总风险在30% - 50%之间。根据术后MR影像,内镜系列手术中69%的患者,以及显微镜系列手术中64.5%的患者,在一开始手术中完全切除肿瘤。即使在经影像学证实的完全切除垂体腺瘤的情况下,仍有长期复发的风险。Reddy等人报道,6.9%的完全切除患者平均复发时间为9.1年。重要的是,在这项研究中,20%的再生长发生在10年的随访之后。很明显,在这些病例中,单独长期和或许终身观察是治疗策略的选择,有可能再次手术也会复发。
然而,不完全切除有很高的复发率;这取决于残留病变的体积,15%的鞍内残留肿瘤在5年内生长,相比之下,51%的鞍外残留肿瘤在5年内生长。这使得一些中心在有肿瘤残留的区域采用常规的术后放疗
肿瘤复发的因素有哪些?
①完整切除术的解剖学限制因素
能否完全切除肿瘤取决于多种因素,包括肿瘤的异质性和侵袭性。许多放射影像学特征是手术结果不佳的标志,如多叶的较大腺瘤、骨质侵袭和海绵窦受累。对功能性和无功能性腺瘤(表1.图1)两者,改良Knosp分级是一个用来评估肿瘤切除率的有用的工具,它描述了腺瘤与颈动脉的关系。
表1.垂体腺瘤改良Knosp分级
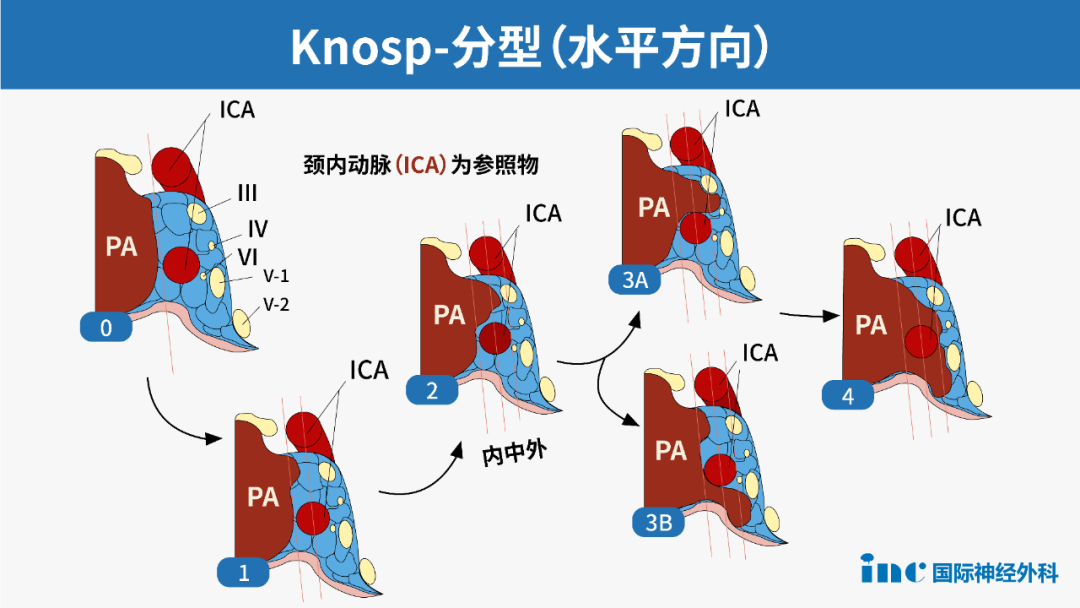
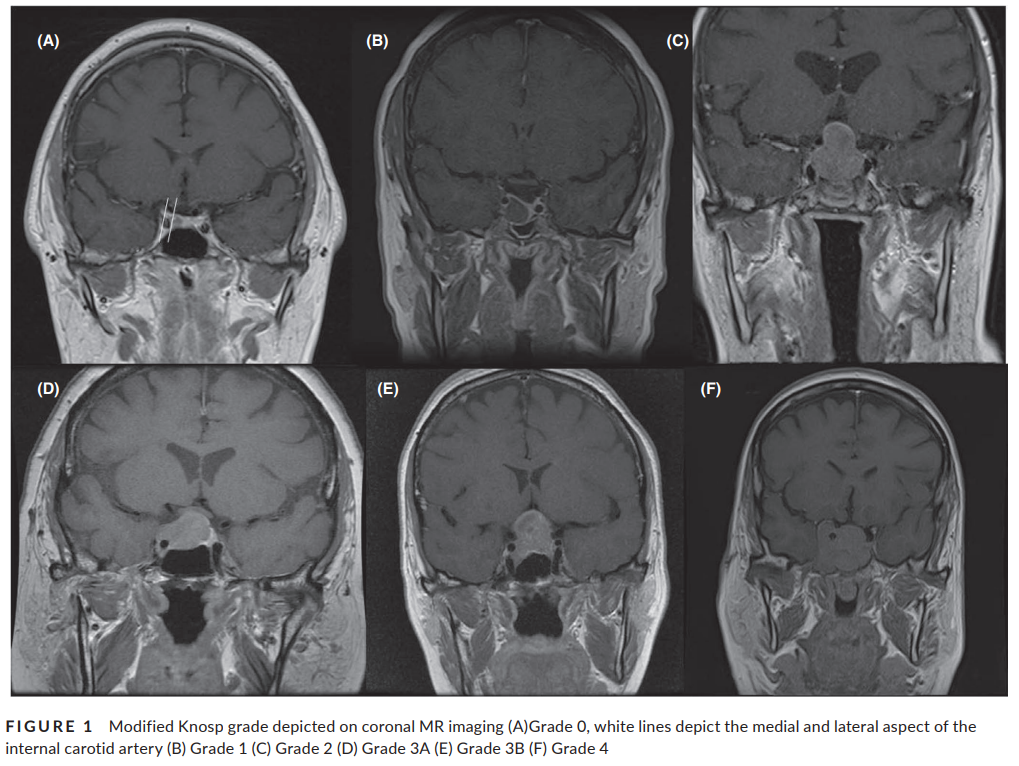
图1 改良Knosp分级冠状面MR成像(A) 0级,白线描绘颈内动脉内外侧,(B) 1级,(C) 2级,(D) 3A级,(E) 3B级,(F) 4级。
②侵袭性垂体腺瘤难以全切
已证明,大多数垂体腺瘤表现出良性特征,多年来复发率缓慢,其自然史受手术切除的解剖学限制因素所支配。然而,有一些腺瘤亚型表现出快速复发和对治疗的抵抗耐药性。许多中心认为Ki-67 为7% -10%更与临床相关,可评估进袭性行为。在目前的分类中,虽然Ki-67仍然是进袭性行为的重要标志,但没有定义阈值,肿瘤侵袭(海绵窦或斜坡侵袭)的额外证据也应被视为临床进袭性行为的标志(表2)。
表2.进袭性垂体腺瘤的影像标志

重要的是,一些变异的腺瘤被发现具有较强的进袭性临床行为,包括稀疏颗粒性生长激素细胞腺瘤,静默性促肾上腺皮质激素细胞腺瘤,新的疾病实体多激素PIT-1阳性腺瘤,以前称为静默性亚型3腺瘤(表3)。
表3.垂体瘤复发可能性

4. 垂体瘤复发后该怎么治疗?术后再手术的重要意义?
复发性腺瘤的重复手术的作用还没有得到很好的研究。由于视角的好转,更好的照明,对关键神经血管结构和正常垂体的识别的改进,加上使用成角度内镜进入海绵窦的能力,内镜方法的广泛采用近期增加了对较大化肿瘤切除潜力的关注。显微入路后腺瘤残留率高的一个因素是有限的蝶鞍和鞍骨暴露,很难进入鞍区和鞍上区域。内镜入路可广泛切除鞍底,显露海绵窦壁,借助扩大入路可清楚地看到鞍上池和视觉器官。
然而,垂体术后在手术是具有挑战性的,解剖结构可能会被疤痕组织扭曲。原手术路径和术区瘢痕形成,重要神经血管与肿瘤粘连,肿瘤组织和垂体的界面有时难以分辨清楚,导致再次手术的难度明显高于初次手术,是经蝶窦入路手术,再次手术会导致颈内动脉损伤的风险也明显增加。

根据相关研究,术后再手术后的视力下降的风险更高,先前的放射治疗可以使局部组织去血管化,导致对颅底重建,以防止术后脑脊液漏的选择有限。此外,肿瘤残留通常所在解剖位置不利,但在经验丰富的垂体中心,许多这样的腺瘤可以在考虑其他治疗方案之前,使用扩大的内镜方法手术切除。这就强调了需要有专门的垂体外科医生的三级垂体中心。表4列出了术后再手术的适应证。
表4.术后再手术的指征

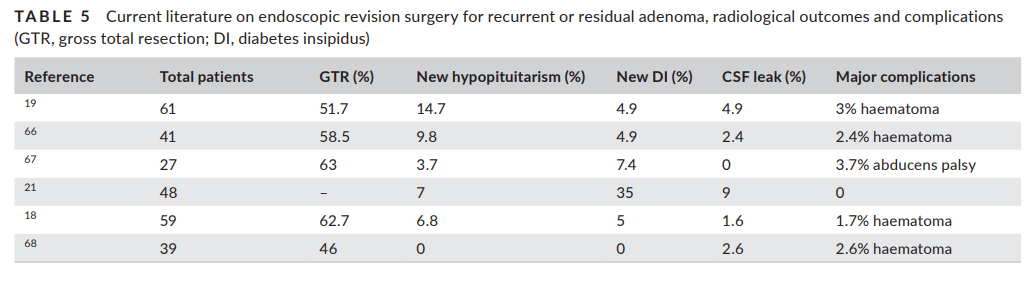
总的来说,无论采用何种手术方式,术后再手术后的大体全切除率(GTR)都低于初次一期手术,术后再手术的全切除率为46.6%-53.5%,而初次一期手术的全切除率为69%-71%。表5总结了目前内镜下术后再手术疗效的经验。Do等报道61例接受内镜下术后再手术的患者。51.7%的患者达到大体全切除(GTR)。海绵窦受累占38%。
表5.目前关于对复发或残留腺瘤内镜下术后再手术治疗、放射影像学结果和并发症的文献(GTR,大体全切除;DI,尿崩症)。
垂体瘤复发再手术的重要意义
虽然重复手术的并发症发生率略高于初次手术,但仍有相当比例的功能性和无功能性腺瘤患者受益。因此,在肿瘤或生化复发的情况下,除非病人不适合手术,或者有解剖学原因限制了成功的可能性,原则是把重复手术作为一选择。
5. 垂体放疗的早期和晚期副作用?是否应避免早期放疗?
放射治疗通常作为功能性和无功能性腺瘤的二线治疗,应用于控制肿瘤和实现生化缓解两个方面。全部类型的放射治疗的目的都是对(残留或复发肿瘤)肿瘤大体体积照射合适的治疗剂量,同时约束对周围正常组织/结构的剂量。
对于任何技术,使用辅助放射治疗都需谨慎地权衡风险。相关研究中垂体瘤放射治疗可能会造成以下危害:
①视神经功能下降、视神经病变风险:
视神经病变的风险在常规放疗(RT)中为1% - 5%,而当视神经的剂量被约束在<10Gy时,在SRS中为1% - 4%。

②垂体功能减退:
据报道在10年以上80%会发生。不同的垂体轴表现出不同的放射敏感性,其中生长激素缺乏症占45%-全切,其次是促性腺激素缺乏症(30%)、促性腺激素缺乏症(25%)和促肾上腺皮质激素缺乏症(22%)。旨在保留正常组织的现代放射治疗技术(调强放疗或SRS)似乎与垂体功能低下较低的发生率有关,垂体功能低下发生率在10%至40%之间。
③增加脑血管事件和认知能力下降的风险:
缺血性卒中尚未被报道为SRS治疗的并发症,但需要较长的随访数据。
④诱发继发颅内肿瘤的风险:
包括胶质瘤、肉瘤或脑膜瘤。Minniti等报道,在20年,继发脑瘤的累积风险为2.4%。然而,SRS和PBT诱导继发肿瘤的风险明显降低。
6. 垂体瘤如何治疗?目前国际治疗指南
在北美和欧洲有一些基于治疗复发性垂体腺瘤和进袭性腺瘤的指南。两者的共同之处是建议这些肿瘤由专门的垂体外科医生进行MDT治疗(表6)。
表6.来自神经外科医师大会(CNS)和欧洲内分泌学会(ESE)的现行关于复发性垂体腺瘤管理的指南摘要。

神经外科医师大会的指南是基于2级和3级证据,建议对术后残留进行早期放疗(CRT或SRS),以减少未来进展的风险。然而,他们承认这一建议是基于有限的证据,并指出手术切除后放疗的时机需要进一步研究。他们还重复切除作为复发或残留腺瘤的主要干预手段,保留CRT或SRS针对手术风险高的患者。
欧洲内分泌学会的进袭性垂体瘤管理指南还建议在考虑其他的治疗方案之前,由专家再次手术,但建议只在在有进袭性行为的临床指标,如肿瘤侵袭性或ki-67高时,对初次手术后残留进行辅助RT。建议对记录到有肿瘤生长的进袭性垂体瘤或垂体癌用替莫唑胺化疗,虽然这是基于低质量的证据。对于该病病程中的哪个阶段应考虑使用TMZ,也没有建议。虽然这两个指南都是基于低质量的证据,但它们为目前的做法提供了一个框架。
7. 总结
进袭性垂体瘤应及早发现,并专门制定治疗方案。在大多数情况下,倾向于考虑早期重复手术,目的在较大限度地顺利切除肿瘤,以对无功能腺瘤长期保护视力和对功能性腺瘤达到生化缓解。在可能的情况下,目的是保持正常的垂体功能,避免放疗,以减少长期垂体功能减退的发生率和降低辐射暴露。患者对术后再手术的耐受性往往比对传统的分割放射治疗的好。在大多数无功能腺瘤中,复发率较低,复发间隔相对较长,可以在一次观察到明显复发后再进行手术。考虑到功能性腺瘤非手术治疗的低治愈率(泌乳素瘤除外),再次手术提供了较好的内分泌缓解机会。
复杂性的复发性垂体瘤应在的垂体中心诊治,从而得到更良好的预后。制定详细周密的手术计划是再次手术成功与否的关键。根据既往手术情况、肿瘤影像学特征和术者经验等综合因素,决定经蝶窦入路还是经颅入路。经蝶窦入路仍然是复发性肿瘤的优选入路;经颅入路则适用于切除广泛累及前颅底、鞍旁和三脑室等处的较大垂体腺瘤。
进袭性垂体瘤通常需要多模式治疗和反复抢救性干预。可能会越来越多地使用替莫唑胺,且在病程中较早使用。然而,手术在减少肿瘤负荷和保持神经功能方面起着关键作用,虽然再次垂体手术仍然具有挑战性。
参考资料:
1.Caroline Hayhurst,et al.Current perspectives on recurrent pituitary adenoma: The role and timing of surgery vs adjuvant treatment
2.中国复发性垂体腺瘤诊治专家共识(2019)
INC国际神外教授在华日程的不断推进,“新生”、“未来”,更多的期待正在落地。关注INC官方账号,后期我们将继续尽快更新巴教授后续中国行的进度。

 胶质瘤
胶质瘤 垂体瘤
垂体瘤 脑膜瘤
脑膜瘤 脑血管瘤
脑血管瘤 听神经瘤
听神经瘤 脊索瘤
脊索瘤




 沪公网安备31010902002694号
沪公网安备31010902002694号