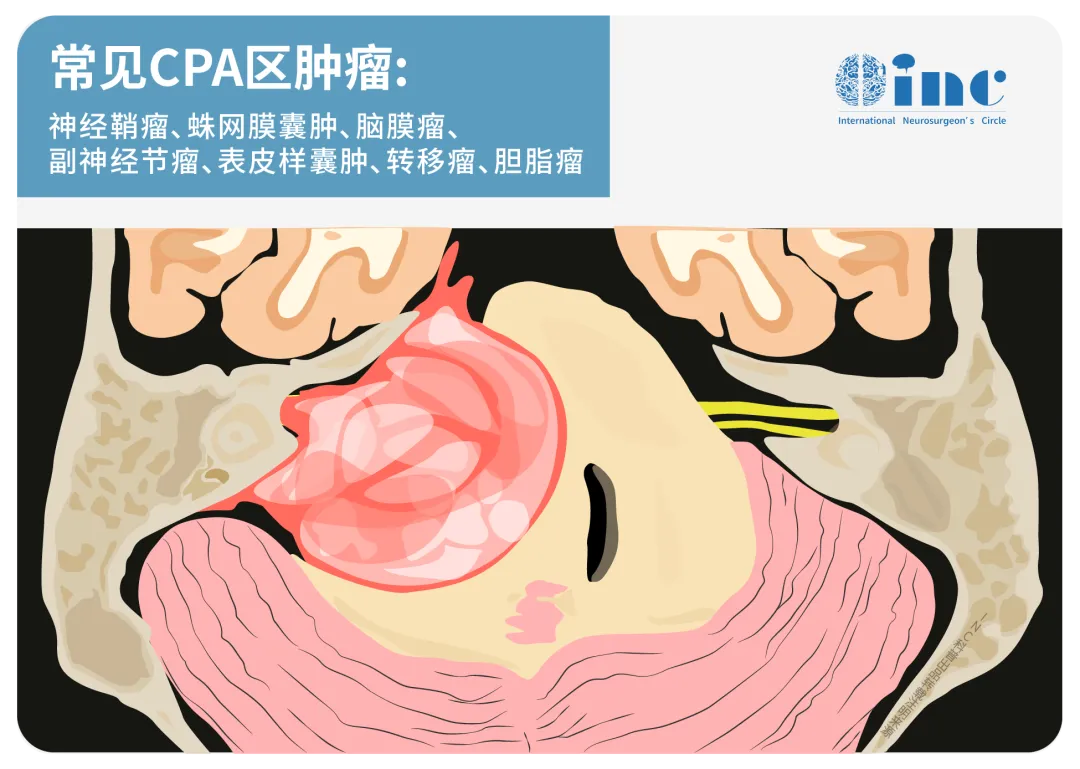
在神经外科领域,桥小脑角(CPA)区域因紧邻脑干且与多组颅神经、重要血管紧密交错,常被称作 “血腥三角”。该区域肿瘤的生长往往导致周围重要结构受压移位或包裹,术中精准识别与保护神经血管的难度极大。若手术操作稍有不慎,可能引发重要血管损伤危及生命,或造成面听神经及后组颅神经损伤,进而导致面瘫、听力丧失等严重并发症。
“医生,这个位置手术风险这么高,能否不开颅?听说可以经鼻切除肿瘤?” 神经内镜是否真的能取代显微镜?事实上,神经内镜与显微镜均为神经外科的核心手术工具,二者并非对立关系,而是需根据病变特征与手术需求选择。每种技术均有其特定的适用场景与优势。
INC 旗下世界神经外科顾问团(WANG)成员、世界神经外科联合会 (WFNS) 颅底手术委员会前主席 Sebastien Froelich 教授(塞巴斯蒂安・福洛里希,简称 “福教授”)在论文《A systematic review on the role of the endoscope in the surgical management of cerebellopontine angle tumors: is it time to draw the conclusion?》中,系统探讨了内镜在桥小脑角肿瘤手术管理中的应用价值与疗效。结论指出,内镜不应作为显微镜的替代工具。这位同时精通显微镜与神经内镜技术的 “双栖” 专家强调,联合运用两种工具可最大限度实现肿瘤的安全切除。

CPA 区肿瘤构成与内镜技术演进
肿瘤构成比例:CPA 区肿瘤中,听神经瘤占比达 75%,脑膜瘤约占 10%~15%,三叉神经鞘瘤、胆脂瘤等其他类型肿瘤约占 10%。
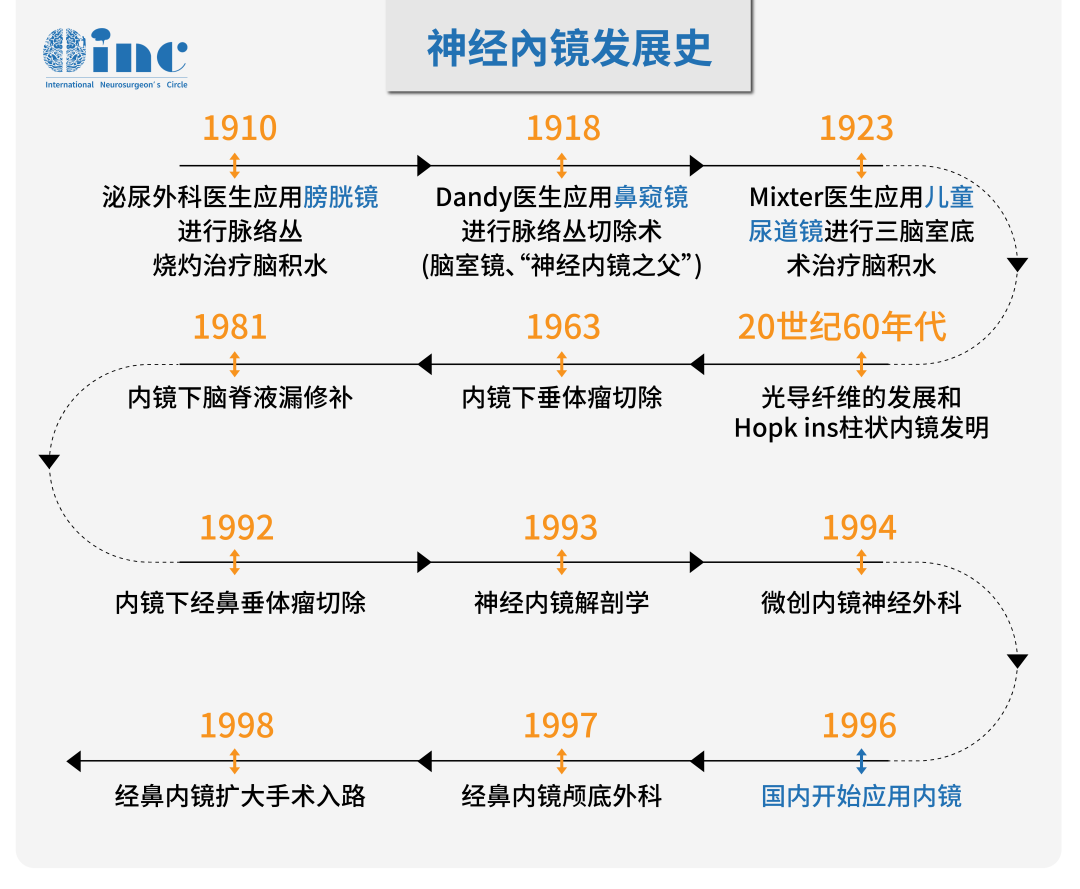
技术发展历程:内镜在小脑后颅窝病变中的应用并非新兴事物,其发展经历了从 “内镜辅助(EA)”(仅作为辅助可视化工具)到 “内镜控制(EC)或全内镜(FE)”(作为全程唯一可视化工具)的重要转变。
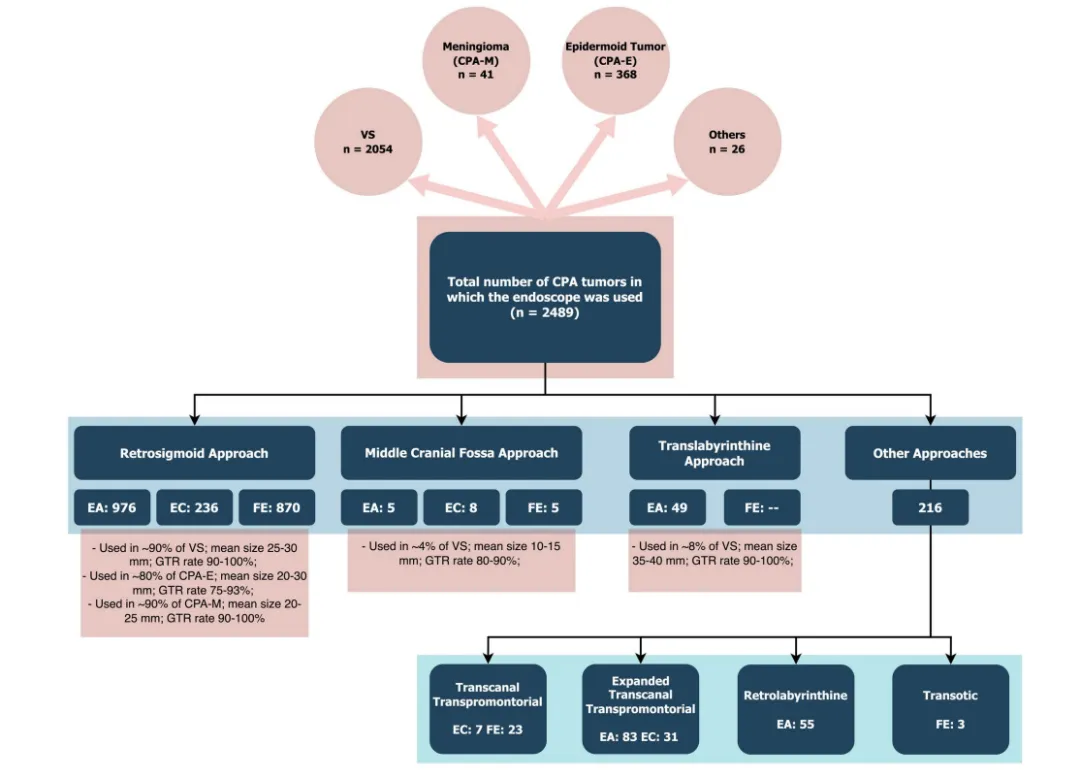
2489 例 CPA 区肿瘤内镜手术研究数据
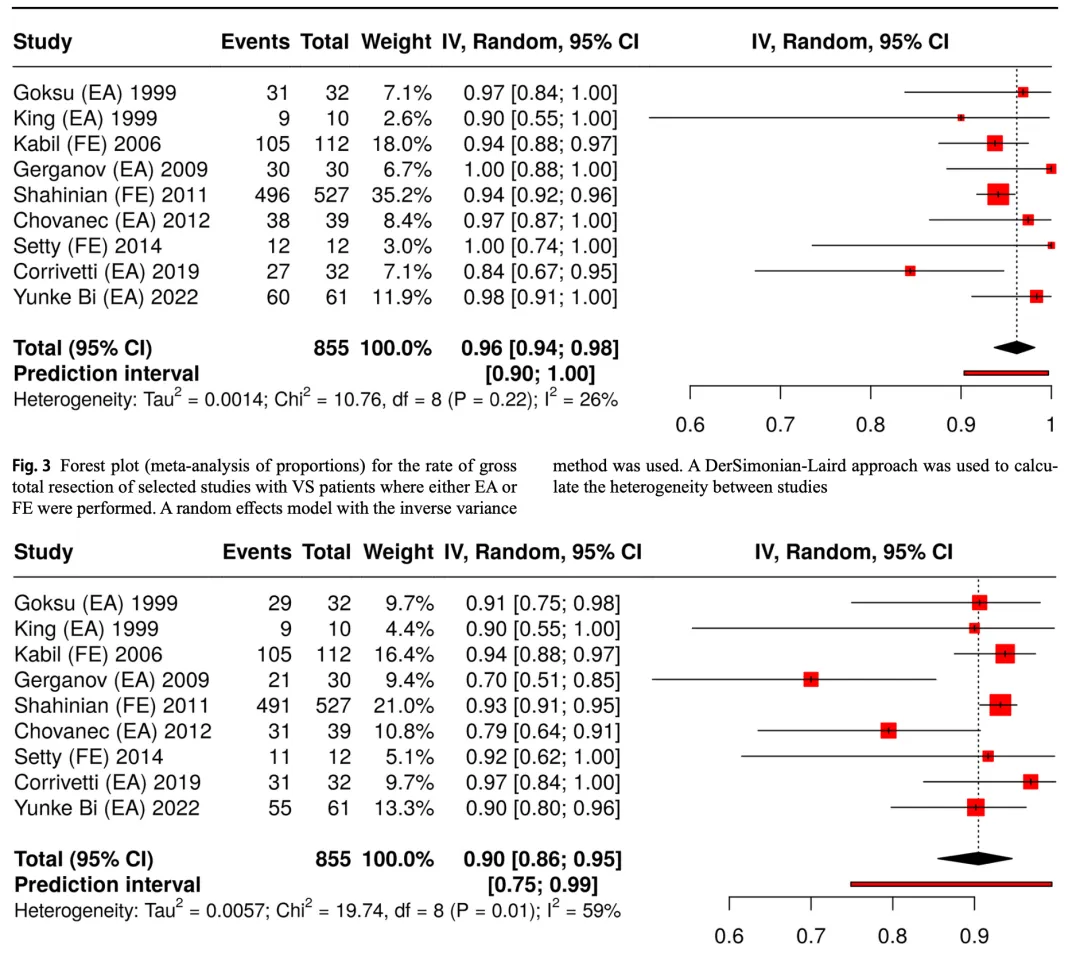
该研究纳入 2489 例接受内镜手术的 CPA 区病变患者,具体病例分布为:听神经瘤 2054 例,表皮样肿瘤 368 例,脑膜瘤 41 例,其他病理类型肿瘤 26 例。乙状窦后入路因其解剖学优势,成为全内镜手术与内镜辅助手术中最常用的入路选择。尽管纳入统计的 1539 例听神经瘤相关研究存在一定异质性,但整体实现了 92.5% 的平均全切除率(GTR),且在 1332 例患者中,90% 获得了良好的面神经功能预后(House-Brackmann 分级≤2 级)。对于 CPA 区脑膜瘤及起源于桥小脑角池的表皮样肿瘤,在内镜辅助下,残留病灶的识别能力显著提升,且未伴随并发症风险的增加。
内镜的核心优势:突破显微镜视野局限
内镜在 CPA 区手术中的关键价值在于增强可视化能力,其斜角光学设计可提供:
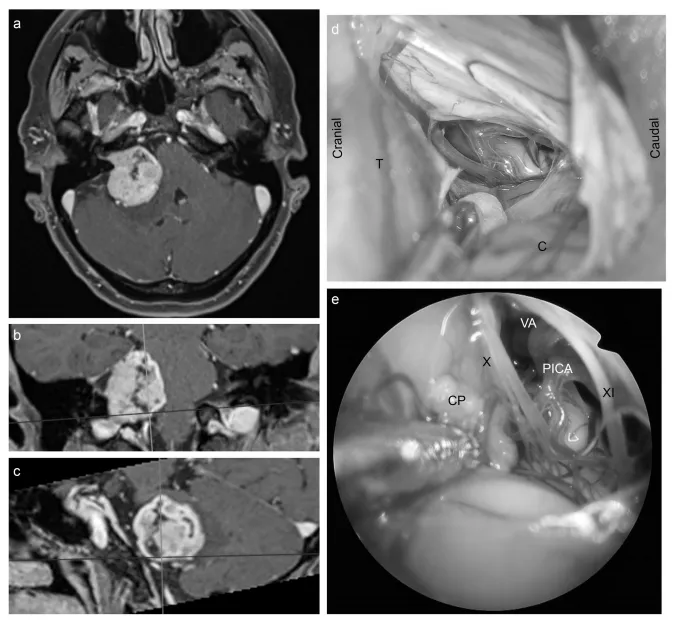
全景化视野:清晰显示脑干水平颅神经连接处、硬膜出入口及血管关系,尤其在狭窄深邃的乙状窦后入路中,可观察到显微镜因直线视野限制而难以触及的 “盲区”(如内听道底部、神经血管结构后方)。
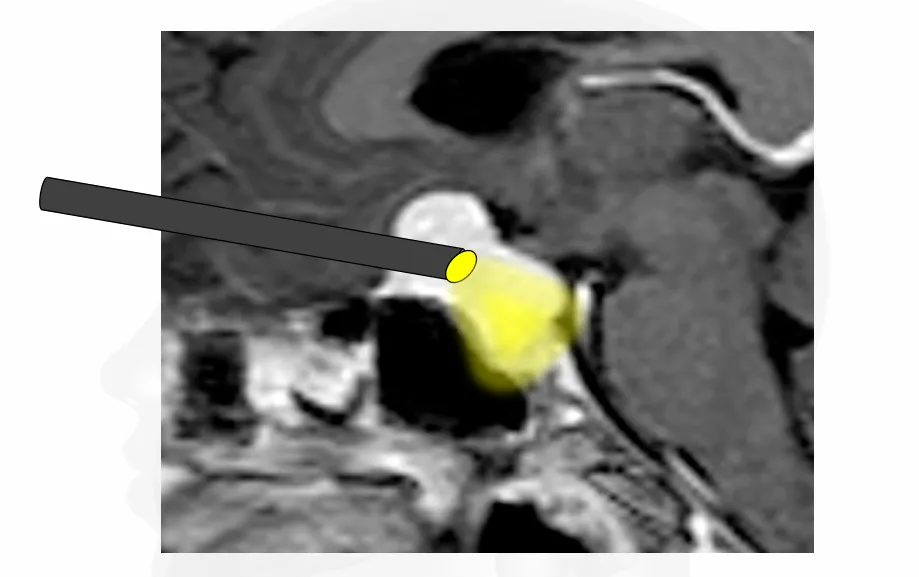
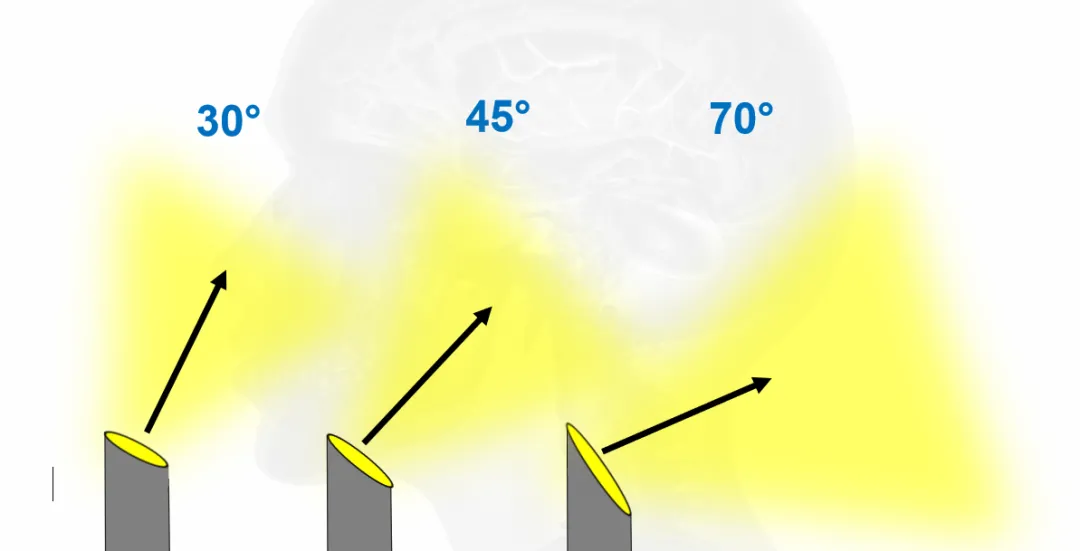
微创化优势:支持小骨窗开颅,减少小脑牵拉程度,同时通过直接观察鼓室降低术后脑脊液漏的发生风险。
精准化评估:在内听道内延伸病变中,内镜可辅助判断肿瘤残留情况,其对囊壁的直接观察较 MRI 更为精准,可识别 MRI 难以显示的微小残留病灶。
内镜技术的局限性与操作瓶颈
三维视觉缺失:内镜操作需动态调整以弥补立体感不足的问题,新手医师易因缺乏三维感知而导致操作困难,3D 高清系统的普及有望改善这一现状。
器械协同难题:较小的手术操作空间可能导致内镜与操作器械相互干扰,需至少 15mm 的开颅空间并结合显微镜引导,频繁进出内镜可能增加神经血管损伤风险。
特殊类型肿瘤限制:
三叉神经鞘瘤因粘连组织与脂肪成分干扰,内镜可视化难度较高;
脑膜瘤因血供丰富、磨除骨屑易堆积,需频繁清洁镜头,影响操作流畅性。
设备与技术门槛:需专业培训与特定设备(如氙灯光源冷却技术以防止热损伤),限制了在基层医院的普及应用。
临床应用建议:双镜联合的协同策略
尽管内镜在 CPA 区肿瘤手术中展现出提升全切除率、优化神经功能保护等优势,但其广泛应用仍受限于技术门槛与传统操作习惯。多数研究表明,内镜更适宜作为显微镜的辅助工具而非替代工具:
显微镜主导操作:用于肿瘤主体切除与关键结构的初步显露;
内镜补充探查:用于探查视野盲区、确认残留病灶、评估神经血管关系。
福教授强调,“双镜联合” 策略可兼顾显微镜的立体感与内镜的广角视野优势,尤其适用于复杂颅底肿瘤的切除。未来随着 3D 技术与机器人辅助内镜的发展,CPA 区手术的精准性与安全性将进一步提升。
结论
在桥小脑角区肿瘤手术中,内镜技术的价值在于补充而非替代显微镜。其增强的可视化能力为残留病灶识别与神经功能保护提供了新视角,但受限于操作复杂性与设备要求,目前更适合作为多模态手术策略的组成部分。对于多数 CPA 区肿瘤(尤其是听神经瘤、脑膜瘤),“显微镜为主、内镜辅助” 的联合手术策略仍是最优选择。随着神经外科技术的持续革新,二者的协同应用将推动 CPA 区手术向更微创、更精准的方向发展。

 胶质瘤
胶质瘤 垂体瘤
垂体瘤 脑膜瘤
脑膜瘤 脑血管瘤
脑血管瘤 听神经瘤
听神经瘤 脊索瘤
脊索瘤




 沪公网安备31010902002694号
沪公网安备31010902002694号