仅需3厘米皮肤切口与1厘米骨孔,即可精准清除脑内病变。一名55岁男性患者表现出脑积水相关症状,包括行走障碍及记忆力减退。经磁共振成像(MRI)检查,发现其第三脑室存在胶样囊肿,并伴有脑室扩张征象。世界神经外科学会联合会(WFNS)内镜委员会前主席Henry W. S. Schroeder施罗德教授采用内镜(LOTTA脑室镜)下切除术处理该第三脑室胶样囊肿,术后3年随访显示无复发。
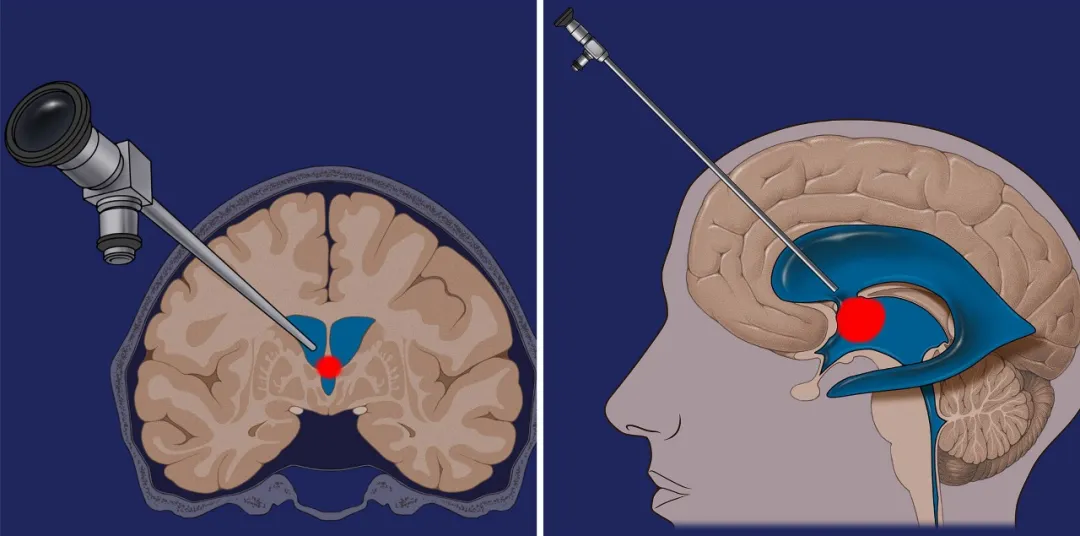
微小颅骨开口即可解决重大脑部病变。人类出生时即具备天然颅骨开口,如前囟门与后囟门,随发育逐渐闭合。颅骨并非完全封闭结构,其底部存在枕骨大孔(连接脑与脊髓的关键通道),以及颈静脉孔、圆孔、卵圆孔等天然孔道,为神经血管提供通路。
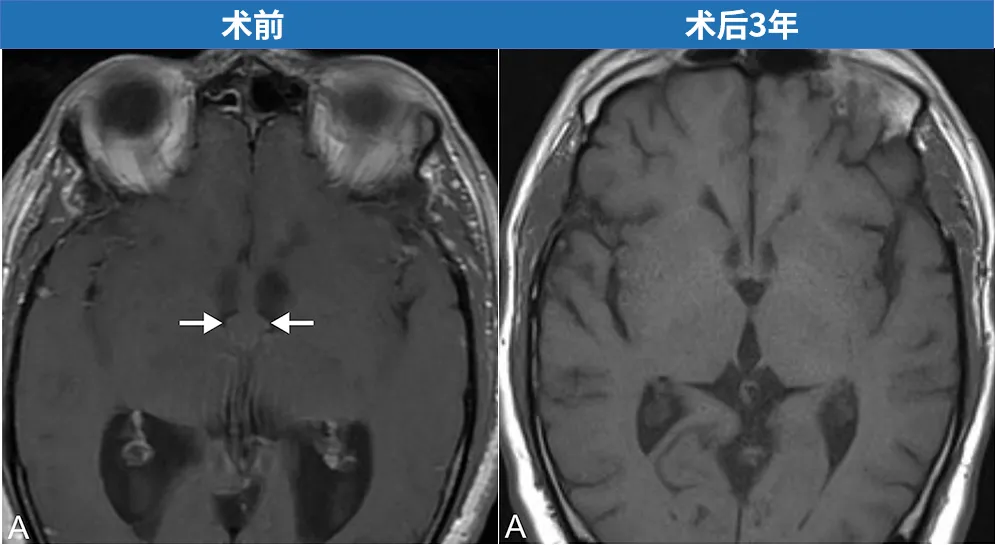
脑部病变切除无需大范围开颅。下文详解Schroeder施罗德教授应用神经内镜清除病变的技术过程。
INC国际神经内镜专家图解病变切除步骤
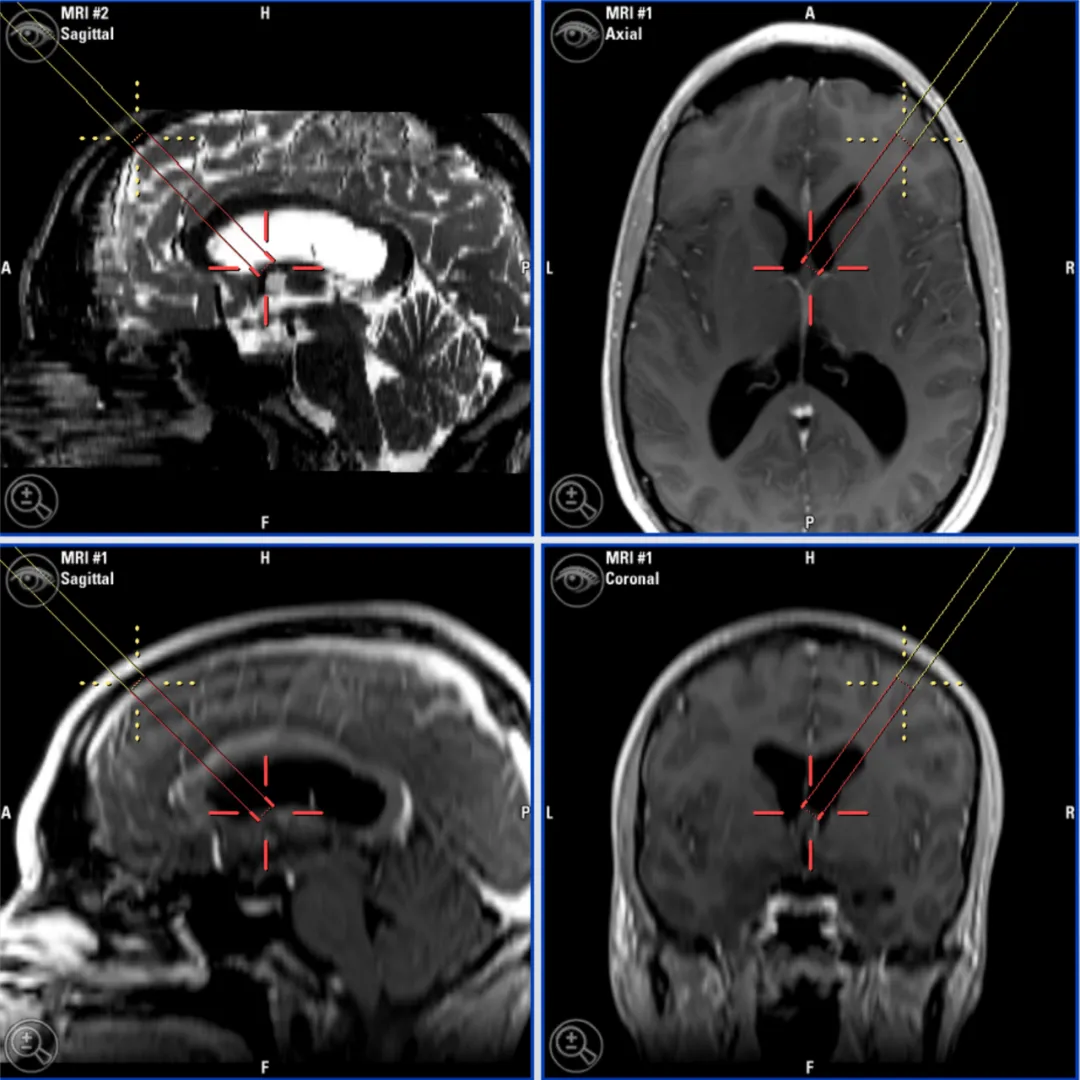
术前磁共振成像(MRI)证实胶样囊肿引发双侧脑室积水。
Schroeder教授演示第三脑室胶样囊肿的内镜下双手锐性切除技术。

手术入路设计
依据磁共振成像(MRI)设计手术路径,避开尾状核头。骨孔定位为冠状缝前4-5厘米、中线外侧4-5厘米。切口选择遵循美容原则:发际线后方或秃顶患者的前额皱纹处。实施3厘米皮肤切口,钻取1厘米骨孔。
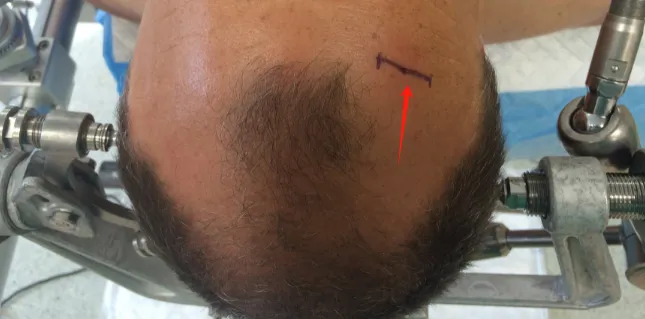
在神经导航辅助下,将带鞘管的LOTTA脑室镜(Karl Storz SE & Co. KG)与穿刺针置入侧脑室额角。
LOTTA脑室镜由Schroeder施罗德教授基于数十年临床经验研发,融合高精度与微创特性。其命名源自教授女儿"LOTTA",赋予技术人文温度。
点击阅读:【不开颅,怎么"钻"进大脑取瘤?LOTTA脑室镜发明者破解脑室手术难题!】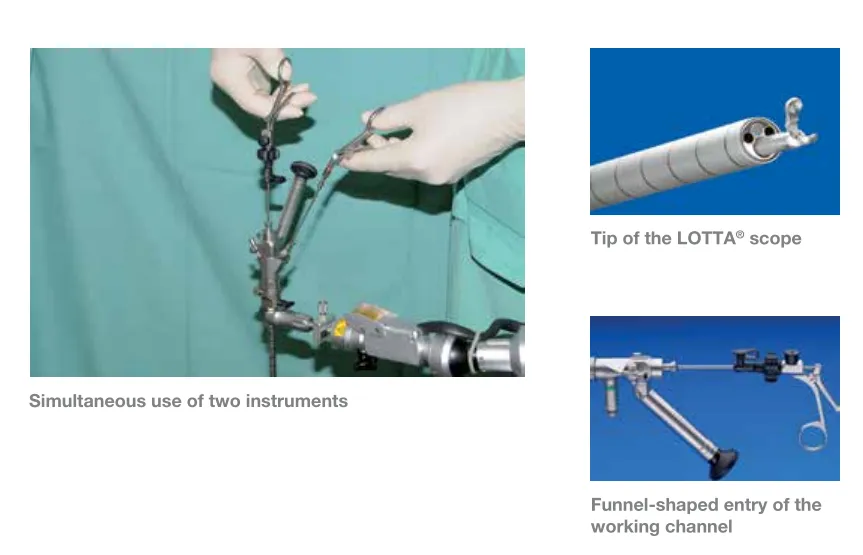
Schroeder施罗德教授依据导航图像规划穿刺路径。实际穿刺轨迹较囊肿真实位置更偏向内上方。进入脑室后,以内镜鞘轻柔下压尾状核头并向外推移,从而优化至囊肿的路径。此法可在保护尾状核前提下,实现最外侧手术通道。
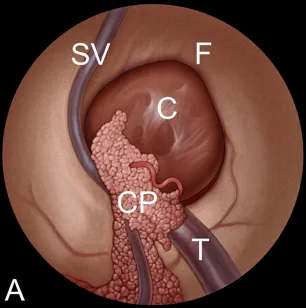
Schroeder施罗德教授图解胶样囊肿切除关键步骤
A:室间孔探查显示胼胝体(F)、脉络丛(CP)、透明隔静脉(SV)、丘纹静脉(T),室间孔受胶样囊肿(C)阻塞。
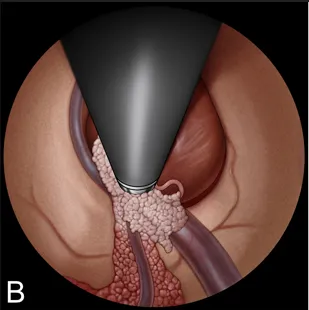
B:双极电凝处理脉络丛。
C:剪刀锐性切开囊肿包膜。
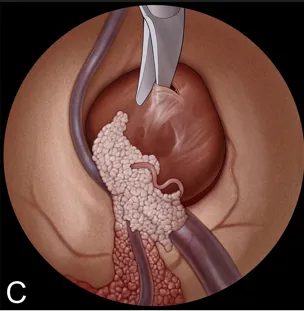
D:吸引管清除囊内容物(右侧为术中实景)。
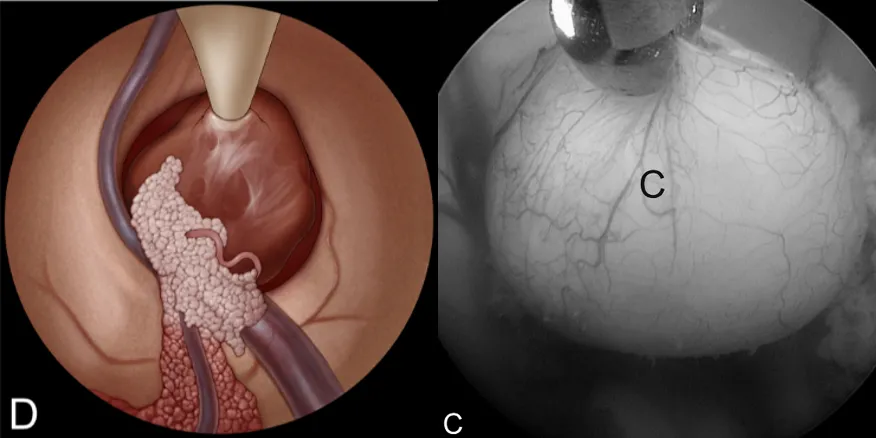
E:囊肿整体移入侧脑室。
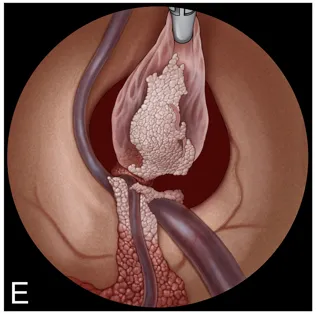
F:双手操作技术暴露囊肿蒂:左通道置入可弯抓钳,主器械经2.9毫米直工作通道进入。
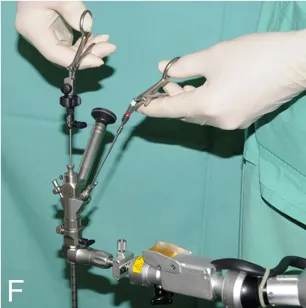
G:双手操作下以双极电凝处理囊肿蒂。
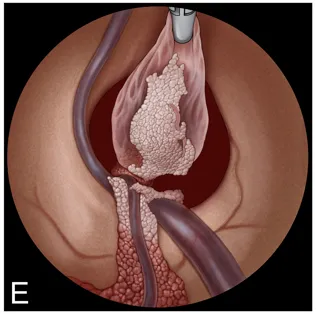
H:双手操作下用剪刀离断囊肿蒂。
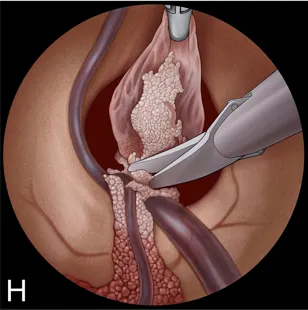
I:切除后复查室间孔。
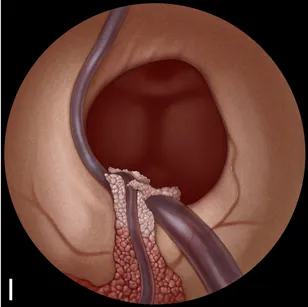
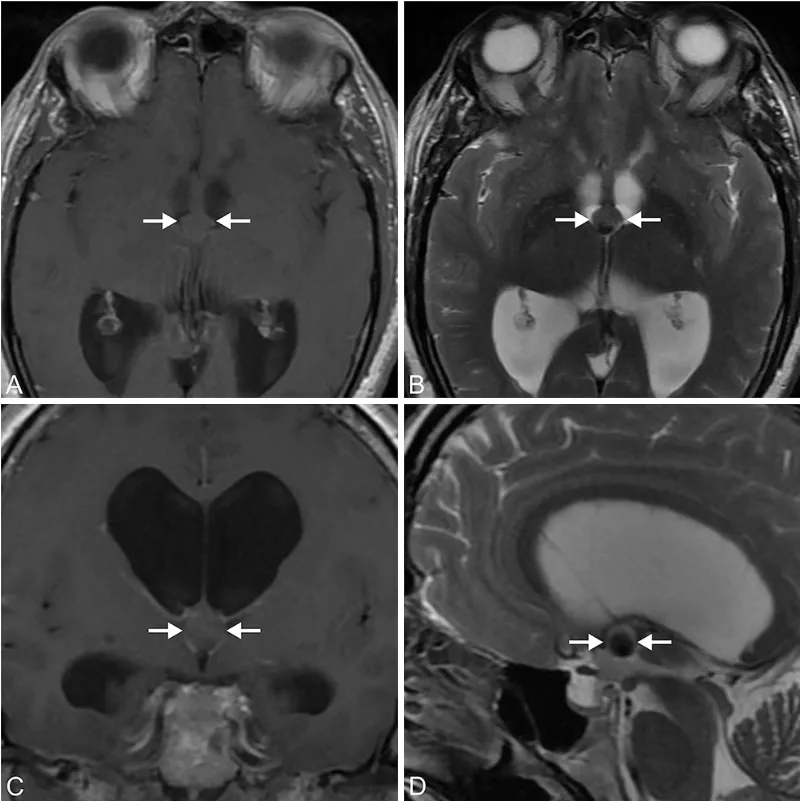
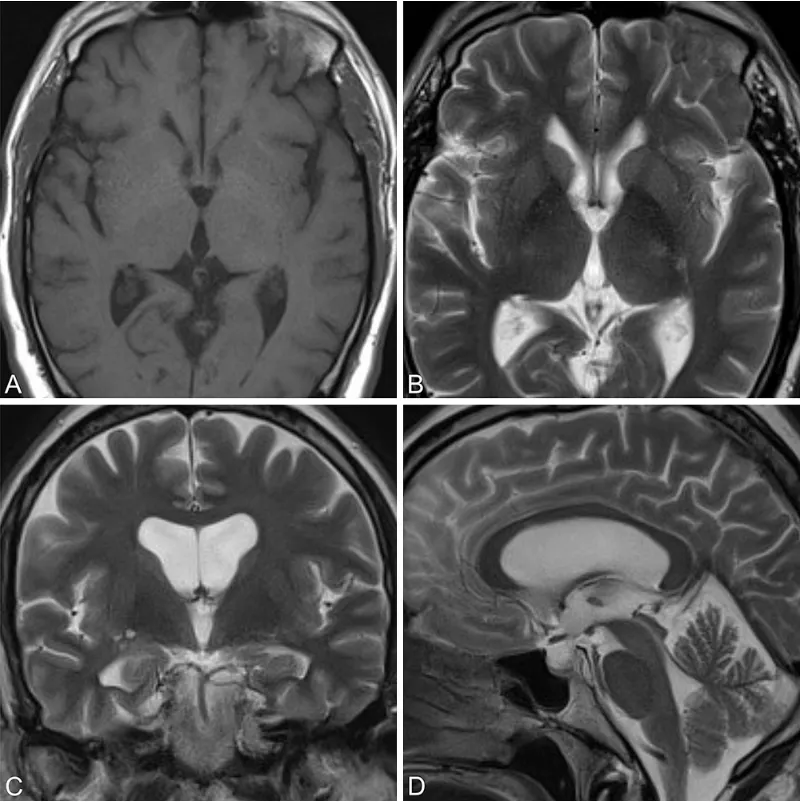
术后3年随访MRI结果:T1加权(轴位A)、T2加权(轴位B;冠状位C;矢状位D)均未见囊肿复发征象。
Schroeder施罗德教授30年技术突破要点解析
第三脑室胶样囊肿属成人原发性颅内良性肿瘤,因位置特殊易引发梗阻性脑积水,严重病例存在猝死风险。当前主要治疗手段为手术,包括显微镜开颅术与神经内镜手术。
神经内镜胶样囊肿切除术历经30年发展,已从单纯囊液抽吸进阶为高全切除率(GTR)、低并发症术式。核心技术创新如下:
01 前外侧穿刺通道
微创理念支持下,单骨孔切除胶样囊肿已成共识。理想穿刺点需满足两点:最小化解剖损伤、最大化全切可能。据此,骨孔定位历经两阶段演变:从传统Kocher点(前冠状缝、中线旁2-5厘米)向更前、更外侧调整。早期入路存在局限:孟氏孔(Monro孔)呈切线位进入,第三脑室顶部囊肿显露困难;穹窿自上而下阻挡,内镜难以无损伤抵达囊肿附着区。
Schroeder教授主张:理想入路点需最大限度外移且避开尾状核头。神经导航引导是实现精准骨孔定位与脑室穿刺的前提,全切除应为首要目标。
02 锐性分离与双手操作技术
传统内镜技术受限于单手操作,仅能完成牵拉、电凝或切割单一动作。单纯牵拉易引发大出血并遮蔽术野,需大量冲洗维持视野。但若缺乏牵引,囊肿易坠入孟氏孔导致蒂部暴露困难。多通道内镜的应用使双手操作技术成为可能,该方案已获多团队验证。
03 内镜手术适应症选择
内镜手术非适用于所有胶样囊肿患者。Schroeder施罗德教授强调需依据个体解剖特征制定手术方案。例如,孟氏孔狭小或脑室发育不良者可能需改用传统显微外科技术。

 胶质瘤
胶质瘤 垂体瘤
垂体瘤 脑膜瘤
脑膜瘤 脑血管瘤
脑血管瘤 听神经瘤
听神经瘤 脊索瘤
脊索瘤




 沪公网安备31010902002694号
沪公网安备31010902002694号