脊索瘤(Chordomas, CHs)是一类组织病理学表现为良性但临床行为具有侵袭性的肿瘤,具有局部侵袭和转移潜能。该类肿瘤的治疗面临重大挑战,最佳治疗方案尚未明确确立。即使采用理想治疗方案,肿瘤复发通常仅能延迟,10-20年后仍难以避免。近年来,随着内镜经鼻入路(Endoscopic Endonasal Approach, EEA)等新技术应用于颅底脊索瘤手术,肿瘤切除范围获得显著改善,这一点至关重要,因为肿瘤完全切除是目前最重要的预后影响因素。
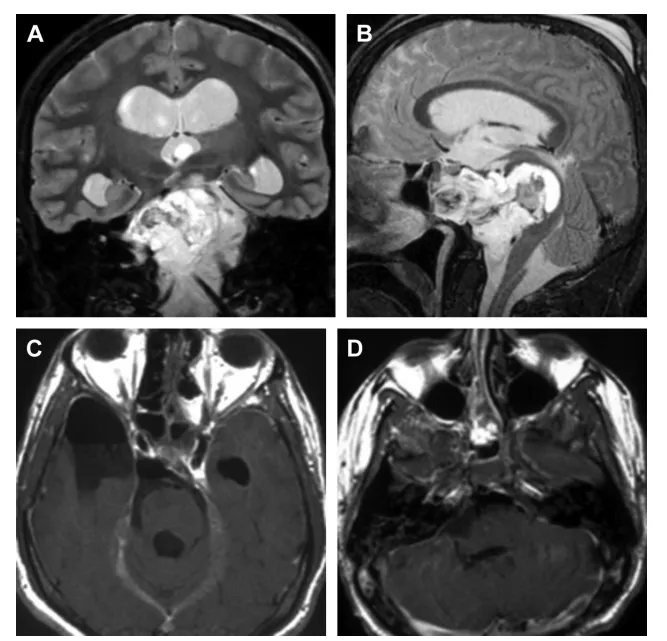
本例复杂脊索瘤病例肿瘤位于关键解剖区域——斜坡上部,且已侵犯硬膜内并深入脑桥。针对这一棘手情况,主刀医师采用三种不同手术入路联合实施的策略:颞颞下入路、颅颈交界区后外侧入路以及内镜经鼻入路。

该病例来源于INC国际神经外科医生集团旗下世界神经外科顾问团(WANG)成员Sebastien Froelich教授(塞巴斯蒂安·福洛里希教授)发表的论文《Chordomas: A Review》。福洛里希教授在论文中深入探讨了脊索瘤的治疗决策策略,重点关注如何通过治疗方案选择为患者争取更佳生存机会。
手术治疗策略与关键技术
外科手术是脊索瘤最有效的治疗手段,肿瘤完全切除仍是影响预后的最关键因素。基于脊索瘤位于中线、起自骨质及硬膜外的解剖特点,不经过颅神经和血管的前方入路成为最符合逻辑且应优先考虑的选择。长期以来,临床主要采用经口、经蝶和经面入路。
目前,内镜经鼻入路(EEA)已逐步取代传统术式。内镜技术可抵达斜坡任何区域——从鞍背(必要时可行垂体移位)至其下缘,甚至可到达颅颈交界区。该入路的侧方界限为静脉结构(海绵窦和颈静脉球)、颅神经及动脉(颈内动脉和椎动脉)。
对经验丰富的手术团队而言,目前已在可接受风险范围内实现侧方颅底区域的抵达,并能在这些重要血管和颅神经周围进行安全操作。在此类情况以及复发性脊索瘤手术中,必须使用微多普勒超声和神经导航技术。颅神经监测(特别是第六、十二对颅神经)为手术切除提供安全保障。球囊闭塞试验可作为术前评估手段,有时可引导术前行载瘤动脉闭塞或术中采取闭塞措施。
内镜技术面临的主要挑战之一是肿瘤侵入硬膜内时的硬膜闭合问题。复发病例的闭合更为困难,因鼻中隔瓣可能无法再次使用。复发病例中,既往放疗史会增加脑脊液漏风险。尽管闭合技术持续改进,术后脑脊液漏发生率仍维持在10%左右。
当肿瘤向侧方侵犯时,可在同一手术或分期手术中联合应用内镜经鼻入路与经颅入路。福洛里希教授的病例中,29.5%采用两种或多种手术入路联合方案。除肿瘤切除外,47例颅颈交界区脊索瘤中有28例需行颅颈固定术。无论采用单一或多重入路策略,对患者而言通常都是严峻考验。
脊索瘤手术策略强调初次治疗时尽可能实现根治性切除。然而,所有病例系列中都包含大量再次手术患者(复发后或初次切除不全后转诊)。福洛里希教授病例中36%为再次手术患者,这类手术难度更大,并发症发生率更高,不完全切除率也更高。
福洛里希教授特别强调初次治疗的重要性,指出初治患者手术相对简单,脊索瘤切除是一次性关键治疗。若首次手术未达到理想效果,后续治疗将面临巨大困难,解剖标志消失等因素将对手术和全切造成重大障碍。
预后影响因素与分子标志物
脊索瘤生长速度影响预后判断,但临床实践中通常难以直接评估肿瘤生长速度。若肿瘤生长缓慢,治疗策略可选择相对保守方案。通过分析患者MRI影像特征可推断生长速度,术前生长速度与术后预后存在关联。大多数病例可通过间隔2-3月的两次MRI检查获得生长速度数据,这一参数对评估肿瘤侵袭性具有重要价值。T2加权像信号特征与约60-70%患者存在关联。

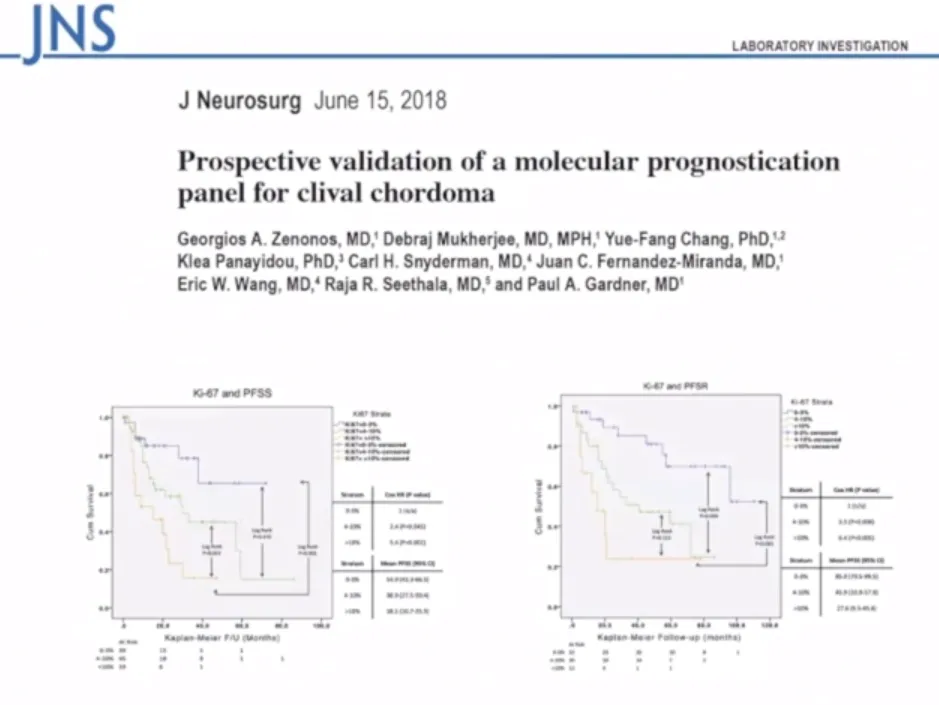
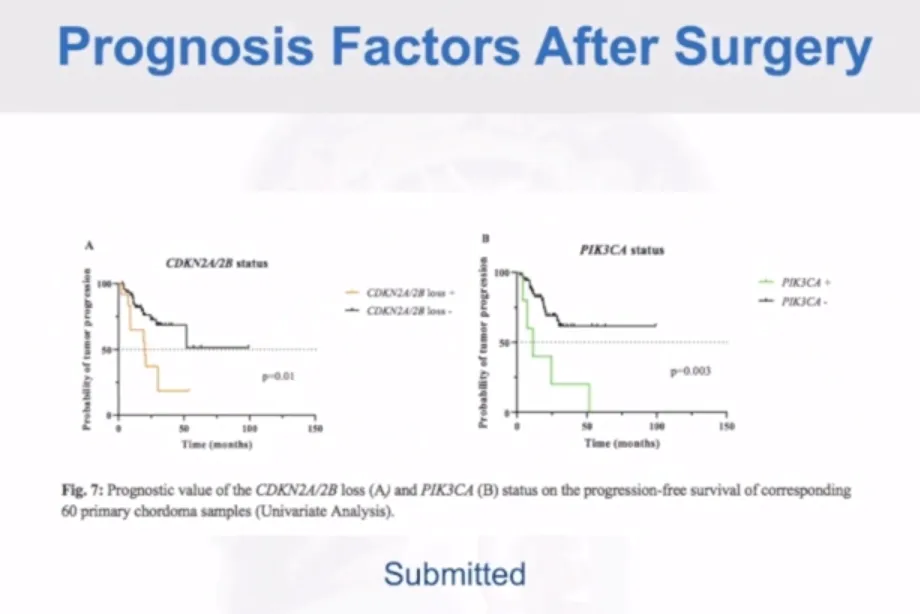
研究发现DNA甲基化与脊索瘤预后存在明确相关性,这为术前评估肿瘤进展速度提供了新方法。另一项研究通过检测1p36和9p21标记物将脊索瘤分为三组,并按不同切除程度进行分层分析。此外,CDKN2A和PIK3CA等分子标记物也具有预后提示价值,这些复杂生物标记物的术前获取是未来重要研究方向。
根据肿瘤生物学行为制定个体化治疗方案:生长缓慢肿瘤可采用相对保守治疗,侵袭快速肿瘤需要积极治疗,术后残留可考虑放射外科处理。成人患者中年龄和性别不影响治疗结果,儿童患者预后较好,但5岁以下儿童预后显著较差。肿瘤部位影响预后,颅底脊索瘤的复发和死亡间隔时间明显长于颅颈交界区和颈椎部位,复发率、转移率和死亡率相对较低。斜坡脊索瘤预后优于颅颈交界区脊索瘤,尽管两者切除率接近。
辅助治疗选择与疗效分析
辅助性放疗的应用价值存在争议,部分研究者仅用于术后肿瘤残留病例,另一些研究者则对所有病例进行术后放疗。已应用的放疗技术包括分次放疗、伽玛刀、射波刀、质子治疗及碳离子治疗。质子与碳离子治疗因生物学效应强大,即使毗邻重要敏感结构仍可给予高剂量照射,通常被认为疗效最佳。
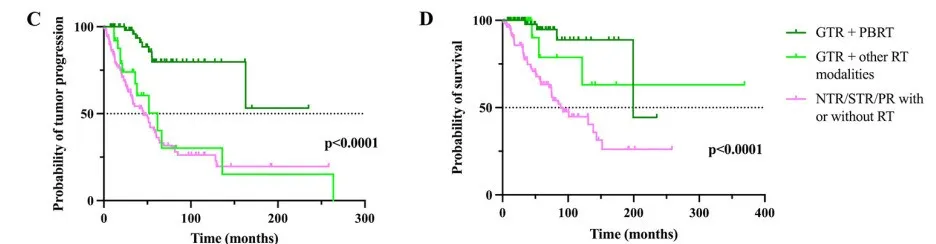
福洛里希教授病例系列中70%应用质子束治疗,精算曲线分析显示手术联合质子束治疗可改善颅底及颅颈交界区脊索瘤的总生存期和无进展生存期,但整体病例系列的益处未达统计学显著性。重要发现是:完全切除联合质子束治疗相比未行质子治疗或不完全切除联合质子治疗,可显著改善总生存期和无进展生存期;平均6.5年随访中,复发率为26%对比50%,死亡率为7%对比50%。
研究数据显示全切除联合质子治疗可获得最佳预后。根据切除范围和辅助放疗的Kaplan-Meier曲线分析:与其他治疗方案相比,接受全切除+质子放疗患者的无进展生存率和总生存率显著更高。
治疗总结与展望
尽管脊索瘤认知取得进展,其仍是治疗挑战性高的致命性肿瘤。肿瘤部位影响预后,颅颈交界区及颈椎脊索瘤预后较差于颅底脊索瘤。目前仍缺乏反映脊索瘤生物学行为的标志物来指导治疗策略调整。鉴于切除范围是最重要预后因素,所有脊索瘤初次治疗均应争取根治性切除。无论切除质量如何,目前常规推荐辅助性质子治疗。
文献来源:
Froelich S, et al. Chordomas: A Review
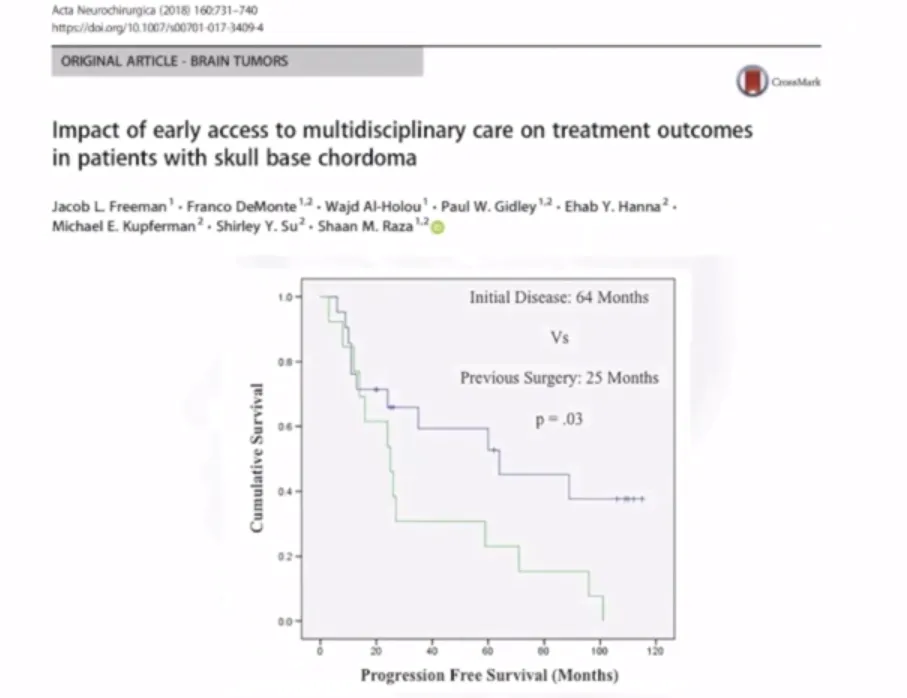
Freeman JL, et al. Impact of early access to multidisciplinary care on treatment outcomes in patients with skull base chordoma
Zenonos GA, et al. Prospective validation of a molecular prognostication panel for clival chordoma

 胶质瘤
胶质瘤 垂体瘤
垂体瘤 脑膜瘤
脑膜瘤 脑血管瘤
脑血管瘤 听神经瘤
听神经瘤 脊索瘤
脊索瘤




 沪公网安备31010902002694号
沪公网安备31010902002694号