是否切除脑瘤必须进行大范围开颅?
通过眉弓处微小切口进入颅内,显微镜提供精准通道,随后引入神经内镜,可直接探查传统手术的视野盲区,使深藏颅底的残余肿瘤充分暴露!一例颅底脑膜瘤患者通过眉弓入路联合内镜技术,在完整保留视神经功能的同时实现肿瘤全切,术后39个月随访未见复发。
该案例由INC国际神经内镜权威专家、世界神经外科学会联合会(WFNS)内镜委员会前主席Henry W.S. Schroeder教授(施罗德教授)于2011年发表于《Neurosurg Rev》。

颅底脑膜瘤因其与重要神经血管结构紧密相邻且手术路径受限,始终是神经外科领域的挑战性病变。肿瘤常沿颅底广泛生长,易累及关键血管与神经;部分病灶常被颅底骨性突起及神经血管结构遮挡,显微镜的直线视野难以充分显露,往往需要广泛磨除颅底骨质并牵拉脑组织及神经血管。而内镜技术的应用,为外科医生提供了多角度观察能力,无需过度操作即可探查手术死角,有助于实现肿瘤的安全全切!
施罗德教授在早期研究中即发现,在经颅入路切除颅底脑膜瘤过程中,内镜辅助技术能显著提升显微镜的效果,实现微创性与根治性的理想平衡。
内镜辅助技术在颅底脑膜瘤显微切除术中具有重要价值:
通过较小的骨窗即可探查显微镜直视范围外的死角,提高肿瘤切除率;
在常规骨窗及颅底入路中,利用不同角度内镜可绕过骨性结构、硬膜及神经血管,减少颅底骨质磨除和脑组织牵拉,从而降低手术创伤。
简言之,若发现显微镜视野下存在残余肿瘤,可引入内镜,在内镜直视下进一步切除。
经眉弓入路双镜联合实现肿瘤全切 术后39个月随访无复发
在处理前颅底肿瘤的经眉弓入路中,内镜技术不仅极具价值,有时甚至是实现全切除(GTR)的必要手段。鞍结节(TS)脑膜瘤起源于鞍结节的硬膜,尤其多见于视神经管和视交叉沟外侧的交界处(最常见起源部位)。视觉障碍是其常见的临床表现,发生率高达80%,这与鞍结节和视交叉之间密切的解剖关系相关。鞍结节脑膜瘤起源于视交叉下方,随着肿瘤增大,会向上、向外侧推移视神经,并且约67%的病例肿瘤会侵犯视神经管,导致视力下降和视野缺损。
55岁女性患者,因视野缺损及视力减退被诊断为鞍结节脑膜瘤,如何在保全神经功能的前提下实现肿瘤全切?
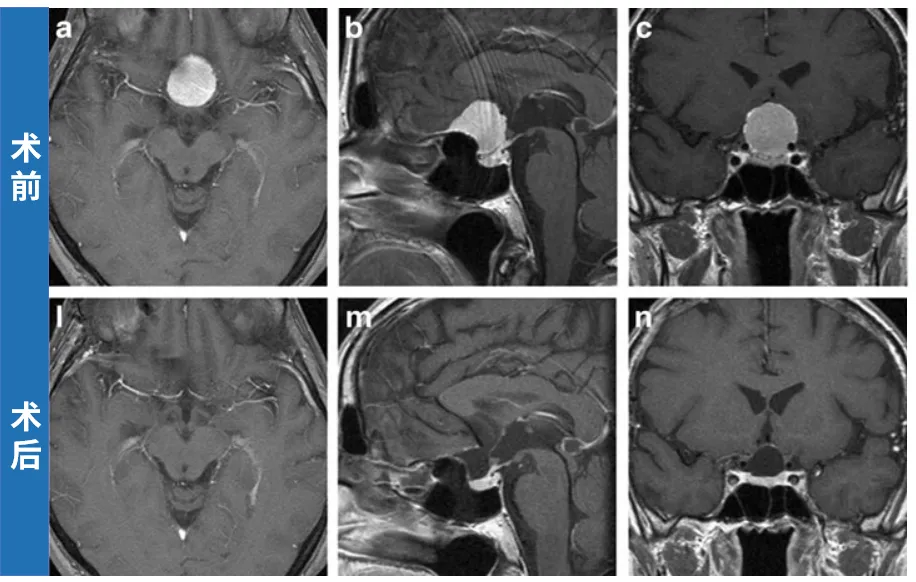
a--c 术前增强T1加权MRI,均显示鞍结节脑膜瘤
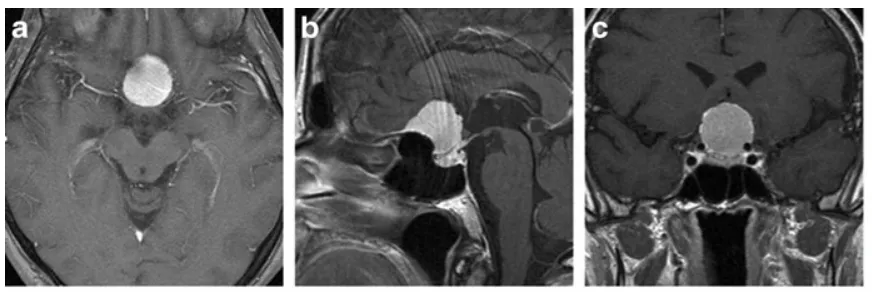
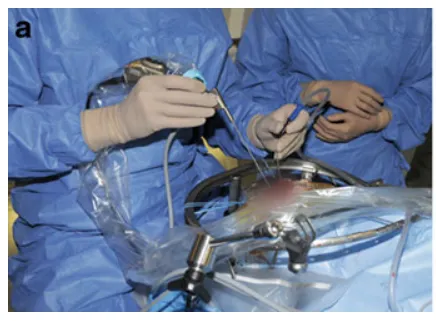
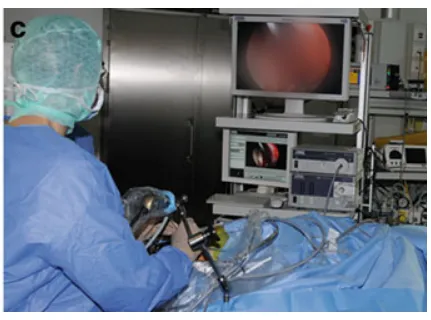
手术具体操作:
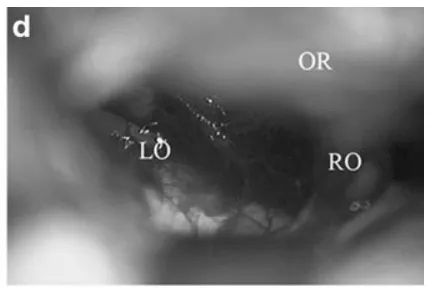
d 显微镜下经眉弓入路所见:可见左侧(LO)及右侧(RO)视神经;因眶顶(OR)遮挡,鞍膈未显露。
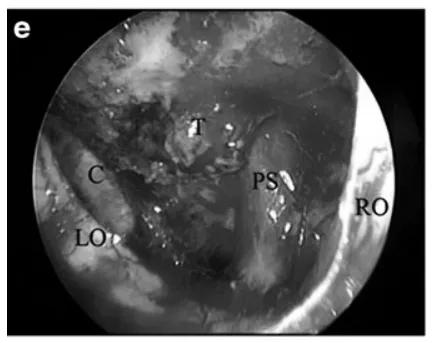
e 30°内镜探查所见:可见左侧颈内动脉(c)、左视神经(LO)、右视神经(RO)、垂体柄(PS)及显微镜无法观察到的残余肿瘤(T)。
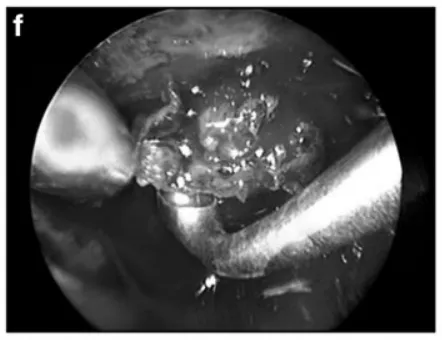
f 内镜辅助下双手操作(bimanual)切除肿瘤。
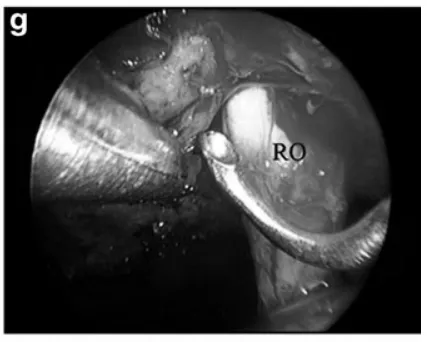
g 于右视神经(RO)内侧继续切除肿瘤。
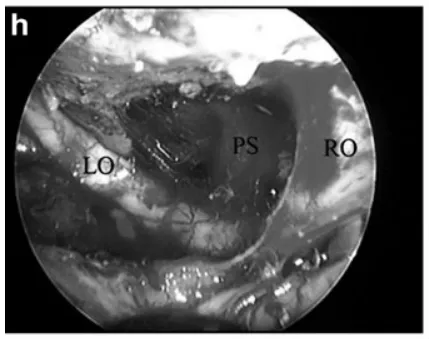
h 内镜下全切后所见:左视神经(LO)、右视神经(RO)及垂体柄(PS)均保持完整。
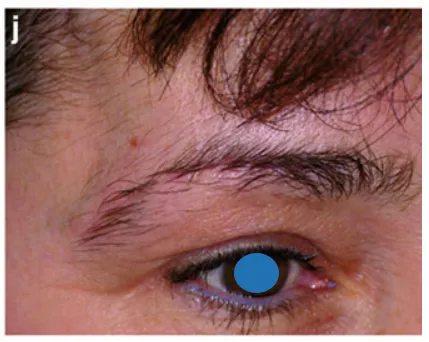
j 术后4个月外观照片:切口美容效果满意。
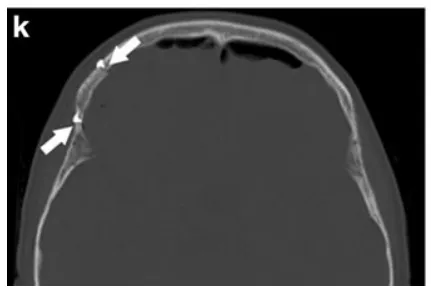
k 术后CT:显示骨窗范围(箭头标示)
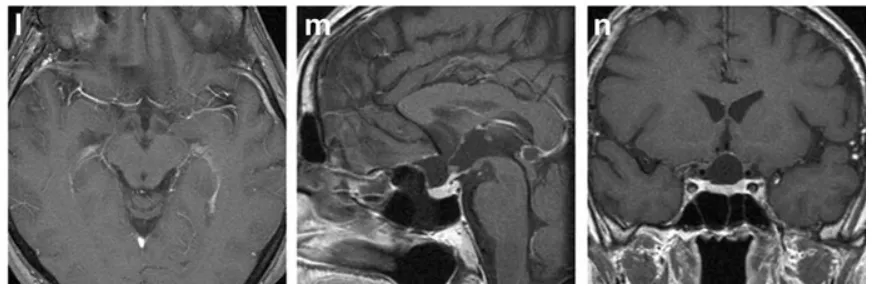
l--n 术后39个月增强T1加权MRI,均未见肿瘤残留或复发征象
颅底手术的“优势组合”显微镜与内镜联合应用,精准切除脑瘤!
内镜辅助显微外科技术切除颅底脑膜瘤,有机整合了手术显微镜与内镜的优势。
手术显微镜可提供出色的三维立体视野,对于位于直线视野内的肿瘤部分,显微镜凭借其高分辨率、优异色彩还原及立体视觉,仍是理想的可视化工具。而当需要探查“转角后方”区域时,则引入内镜,以减少脑组织牵拉和颅底骨质磨除范围。
显微镜在深部狭窄术野存在照明局限与视野盲区;内镜则提供多角度探查能力
在深邃狭窄的手术通道中,显微镜的照明常显不足——入射光在入口处即发生衰减,到达深部术野时亮度显著降低。更为关键的是,显微镜仅能提供直线视野,任何被遮挡的结构均成为视野盲区。而内镜如同具备广角视野的探查工具,在狭小的颅底空间内可实现多角度观察,甚至能清晰显示偏离镜轴方向的病灶,使隐藏的肿瘤充分暴露。
利用不同角度(0°、30°、45°、70°)的内镜,术者能够探查位于神经血管结构后方的区域,这一特性在颅底手术中优势显著。内镜可将光源直接贴近目标区域,为深部术野提供均匀、充足的照明;同时,内镜具有较大的景深范围,高倍放大时也较少需要反复调焦,性能优于显微镜。
当然,内镜也存在局限性。其主要缺点为缺乏真正的三维深度感知。虽然可通过训练利用“鱼眼效应”造成的图像畸变及运动视差(近处物体移动幅度大于远处物体)带来的视觉提示,在一定程度上弥补立体视觉的缺失。
综上所述,显微镜+神经内镜“双镜联合”策略使得即使存在显微镜直线视野盲区,颅底脑膜瘤也能被安全切除。在显微手术过程中应用内镜,可缩小骨窗范围、改善深部照明与视野显露,并允许术者绕过骨性突起及重要神经血管结构进行观察,从而避免或显著减少对颅底骨质的磨除以及对脑组织的牵拉。在神经外科手术中,将两者优势结合应用,是合理的选择。
INC国际内镜权威专家


 胶质瘤
胶质瘤 垂体瘤
垂体瘤 脑膜瘤
脑膜瘤 脑血管瘤
脑血管瘤 听神经瘤
听神经瘤 脊索瘤
脊索瘤




 沪公网安备31010902002694号
沪公网安备31010902002694号