脑动脉瘤是一种位于大脑血管上的异常膨胀或突起,通常发生在动脉壁的薄弱部位。随着血流的冲击,动脉壁的薄弱区域会逐渐鼓起,形成动脉瘤。脑动脉瘤的大小和形状各异,小到几毫米,大到几厘米。
脑动脉瘤可能终身无症状,但也有可能发生破裂,导致严重的出血(如蛛网膜下腔出血),甚至危及生命。
脑动脉瘤的类型根据形状和位置,脑动脉瘤主要分为以下几类:
1、囊状动脉瘤:较为常见,通常呈球形或椭圆形,类似于一个小囊状结构,多见于大脑基底动脉附近。
2、梭状动脉瘤:动脉管壁局部扩张呈梭状,通常沿动脉的整个壁部扩张,较少见。
3、夹层动脉瘤:动脉壁的内膜和中膜分离形成的瘤体,与血管壁的撕裂相关,通常较为危险。
脑动脉瘤的形成原因尚不完全清楚,但通常与以下因素相关:
1、遗传因素:某些家族中动脉瘤的发生率较高。
2、高血压:高血压增加了动脉壁的压力,使动脉瘤更易形成。
3、动脉硬化:血管壁因硬化而变薄,增加了形成动脉瘤的风险。
4、先天性血管壁异常:有些人出生时血管壁较薄弱,容易形成动脉瘤。
在我们往期的文章中已多次提到动脉瘤(具体可至文末查看相关链接)。生长于不同位置的动脉瘤其特征、破裂风险、手术治疗策略也不尽相同。
大脑后动脉(PCA)动脉瘤是一种位于大脑后动脉上的动脉瘤,实为罕见,占脑动脉瘤的不到 2%,而 PCA 动脉瘤(PCAA)有 25% 以上为梭形动脉瘤。
PCA动脉瘤的形成原因与其他类型的颅内动脉瘤相似,包括动脉壁的先天性薄弱、高血压、动脉粥样硬化以及某些遗传因素。这些动脉瘤可能会膨胀并有破裂风险,导致蛛网膜下腔出血(SAH),危及生命。
大脑后动脉供应大脑的枕叶、颞叶和一些深部结构,控制视觉处理和记忆等功能。PCA动脉瘤虽然较为少见,但因其位置复杂,容易引发严重的神经系统并发症。PCA动脉瘤的症状与动脉瘤的大小、位置及是否破裂有关。常见症状包括:
头痛,特别是剧烈的“爆裂样”头痛
视力障碍,如视野缺损、双视等
恶心、呕吐
面部或四肢麻木、无力
神志改变,甚至昏迷(尤其在动脉瘤破裂时)
PCA起源于基底动脉(BA)末端,通过后交通动脉(PCoA)提供前循环的侧支血液供应。PCA动脉瘤的解剖位置较深,正确认识和理解PCA的显微外科解剖和血管区域是安全有效治疗动脉瘤的基础。
在过去 30 年中,血管内治疗技术发展迅速,靠近脑干 PCA 动脉瘤多采用血管内技术治疗。但是,单纯的血管内治疗可能带来较高的缺血性卒中的风险,如果结合血运重建则可以有效防止并发症的发生。
旁路手术结合近端闭塞或动脉栓塞是目前认为治疗复杂 PCA 动脉瘤的有效手段。由于深、狭窄的手术路径和周围敏感复杂的神经解剖结构,PCA 的显微外科操作技术上要求十分严格。

INC国际神经外科医生集团旗下组织世界神经外科专家团(WNEG)成员、国际脑血管搭桥手术大师、日本东京女子医科大学神经外科主任川岛明次(Akitsugu Kawashima)教授尤为擅长动脉瘤的搭桥手术治疗,曾报道过多例施行大脑后动脉P2段动脉瘤孤立术与颞浅动脉(STA)搭桥术,来治疗PCA动脉瘤的经验。

STA-PCA(颞浅动脉-大脑后动脉)搭桥手术是一种用于重建后循环血流的复杂显微外科手术,通常用于治疗大脑后动脉闭塞或动脉瘤等难治性后循环疾病,手术难度大,包括以下几个方面:
1、血管解剖位置复杂
大脑后动脉位于颅底附近,解剖位置深且复杂,邻近多个重要结构如脑干、颞叶和枕叶区域。在操作过程中需要小心避免损伤这些结构,以免引发严重的神经系统并发症。
2、血管直径和吻合技术要求高
STA与PCA之间的直径差异较大。STA较细,而PCA相对较粗,因而进行血管吻合时需要高超的显微外科技术,确保吻合口血流通畅,避免术后出现血栓或狭窄。精准的缝合对于保持血流畅通和减少并发症风险至关重要。
3、供血区域的血流调控
由于PCA供血区域较为重要,尤其是涉及视觉处理的枕叶区域,术中一旦发生短暂血流中断,可能会对患者的视力、认知及运动功能产生影响。因此,术中必须精准控制血流,避免在血管重建过程中引起供血不足。
4、术中操作空间狭小
手术区域靠近颅底,操作空间非常有限,尤其是大脑后动脉的深部位。显微手术环境下,外科医生必须极度小心地操作工具,并充分利用显微镜和其他辅助设备,避免对周围组织的过度牵拉和损伤。
5、术中血管痉挛风险
在STA-PCA搭桥手术过程中,血管痉挛是常见的并发症,可能导致供血不足,影响手术效果。术中处理血管痉挛的措施包括应用血管扩张剂等,但需要小心控制用量,以免影响术后恢复。
6、患者个体差异
患者的血管解剖存在显著的个体差异,特别是在大脑后动脉的分支模式和血管走向上。因此,手术前的精准评估和影像学规划至关重要,需要根据每位患者的具体情况量身定制手术策略。
7、术后管理和并发症控制
术后并发症包括血栓形成、脑水肿、出血、以及新生血管功能不佳等。术后管理至关重要,尤其是血压控制、抗凝治疗和神经功能监测。术后需严格控制血压,并根据患者情况进行抗凝或抗血小板治疗,以减少血栓形成风险。
颞下入路 STA-PCA搭桥重建术——川岛教授案例分享
47岁男性:P1-P2夹层动脉瘤
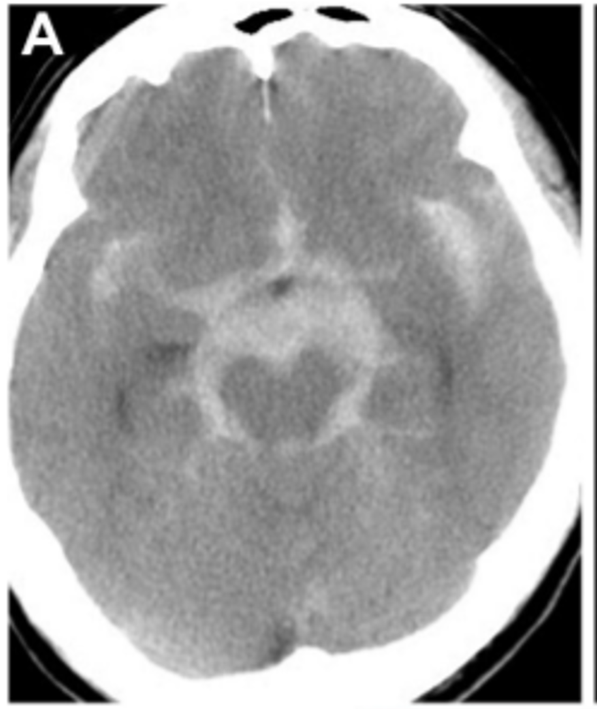
47 岁男性,确诊蛛网膜下腔出血(Hunt-Hess 和 Kosnic 3 级)(图2A)。初次就诊时,3D CTA或DSA未发现扩张或血管病变。
▼CT显示弥漫性蛛网膜下腔出血,尤其是左侧脑桥前池增厚。
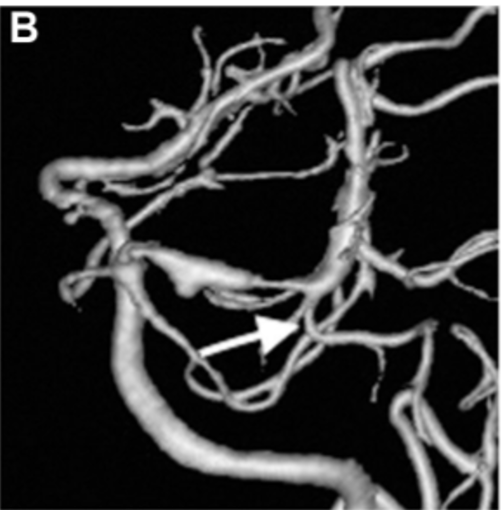
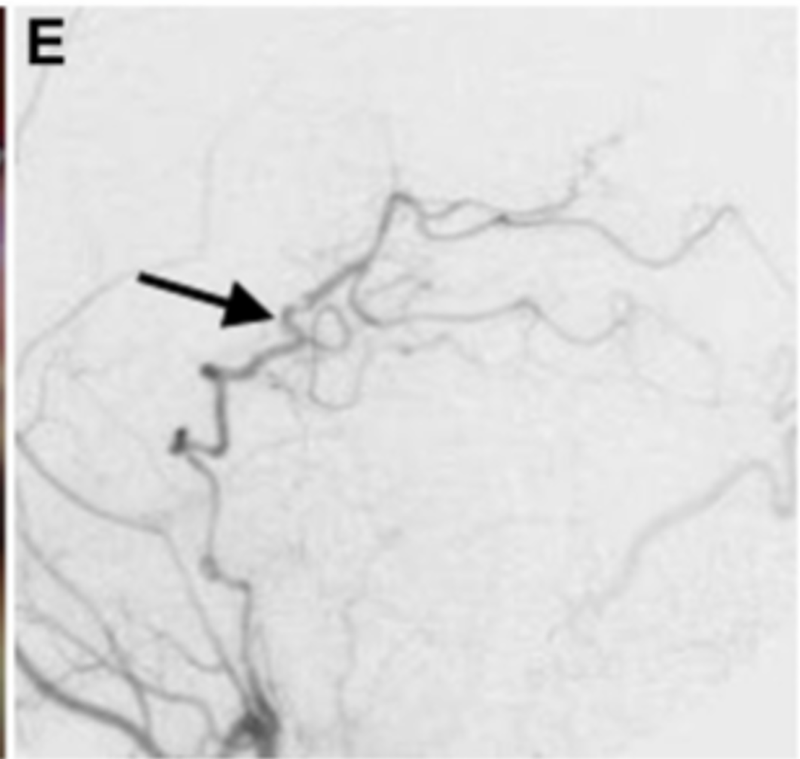
▼出血后第18天的延迟血管造影显示左侧 P1-P2 段有一个不断增长的夹层动脉瘤,并具有狭窄特征(图2B),PTA从狭窄病变的远端部分分支(箭头)。
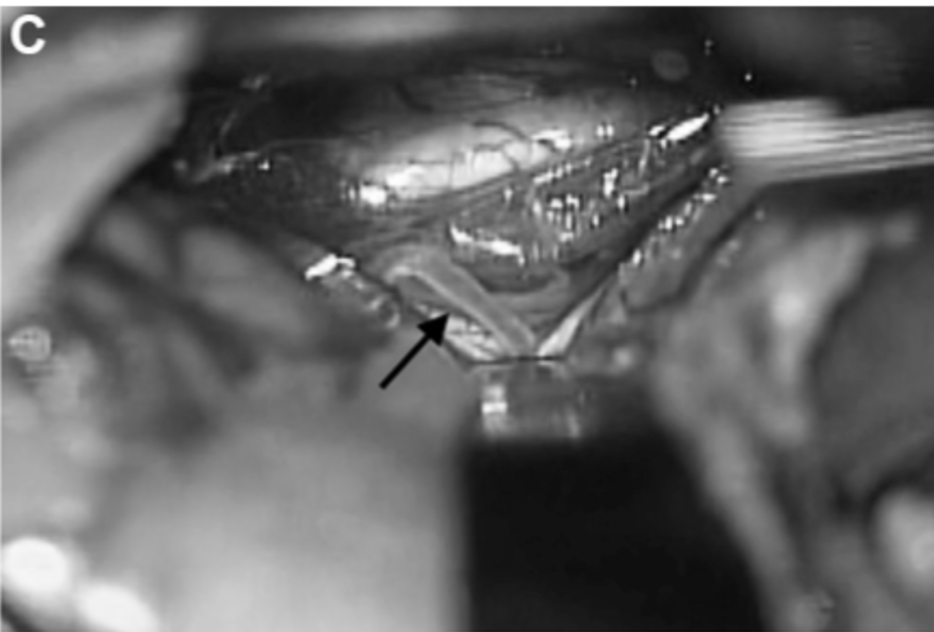
▼第20天,经左颞下入路进行动脉瘤孤立术和 STA-PCA 搭桥重建手术。最初夹闭动脉瘤的近端部分,同时保留丘脑穿支动脉。动脉瘤的解剖区域延伸到P2段后部,就在PTA分支点之前。选择 PTA 作为受体动脉(箭头),因为其口径和角度优于P3段进行吻合(图2C& D)。
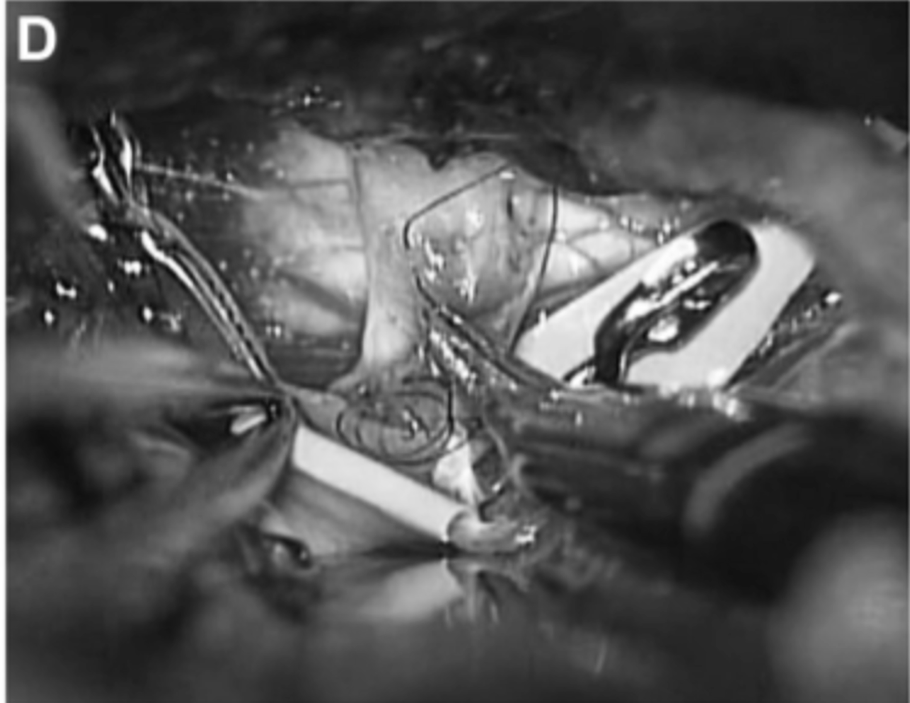
进行 STA-PTA 旁路手术后,川岛教授将远端夹子放置在夹层动脉瘤上,同时保留穿支。术后1周血管造影显示,通过旁路到达左侧 PCA 区域的血流良好,并且动脉瘤完全被排除(图2E)。2周后,患者出院回家,没有出现神经功能缺损。在1年随访中,患者改良 Rankin评分为0.搭桥术仍然有效。
▼术后1周的颈外动脉血管造影显示整个左PCA的旁路血液供应良好(箭头)。
55岁男性:左侧梭形P1-P2交界处动脉瘤
55岁男性,短暂性脑缺血发作和认知功能障碍,影像检查显示右侧颈内动脉严重狭窄,左侧P1-P2 交界处梭形动脉瘤,大小10×12 mm。
患者首先接受了右STA-MCA搭桥术,以预防血流动力学障碍。十月后,患者接受了梭形动脉瘤的治疗(图3A)。
▼A:术前 3D-DSA 显示位于左侧 P1-P2 交界处动脉瘤。B:术后3D CTA显示左侧 PCA 区血管穿支(箭头)和重建的PTA血管(箭头)的血流通畅。
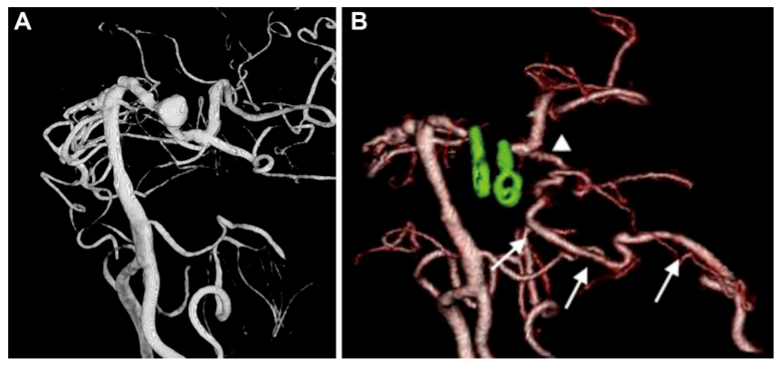
考虑到该患者的大小、位置、壁不规则性以及需要长期抗凝治疗等因素,其发生动脉瘤破裂的风险较高,予以第二次手术。
手术包括远端 PCA 的血运重建和通过颞下入路动脉瘤孤立术。鉴于 P2 远端段严重的动脉粥样硬化变化,选择 PTA 作为搭桥受体动脉。
术后患者出现短暂性失语,1周后完全恢复。手术后1年进行的血管造影显示已排除动脉瘤且左侧 PCA 循环通畅(图3B)。
破裂 or 不破 这是个问题

上述两则案例中,一则属于未破裂动脉瘤,一则已经出现蛛网膜下腔出血。从案例中我们也能发现,一般动脉瘤的结局包括破裂、生长以及保持稳定。
动脉瘤破裂:动脉瘤破裂出血,通常导致蛛网膜下腔出血。多数动脉瘤首次破裂后,原先的破裂口会被血凝块暂时堵住,从而让出血暂时停止,但是这种血凝块是极其不牢固的,如果不经过治疗,已破裂动脉瘤极有可能再次破裂出血,神经损伤及死亡风险极高。
颅内动脉瘤破裂出血的倾向可能与动脉瘤的大小、类型有关。直径小于 4 mm 的动脉瘤壁都比较均厚,不容易破裂出血。
动脉瘤破裂出血主要表现为突然剧烈的头痛、畏光、恶心呕吐、面色苍白并有眩晕、颈项部疼痛。半数的患者会出现精神症状,如烦躁不安等。同时,大部分患者会出现意识障碍,严重者出现昏迷、甚至死亡。
因此,对于有动脉瘤病史患者,出现头痛,尤其是剧烈头痛时,需要警惕是否为动脉瘤复发破裂出血。

动脉瘤生长:动脉瘤在连续观察中可能发生大小、形态上的明显变化,比如动脉瘤在一个方向上增长超过1mm,或在两个垂直方向上各增长超过0.5mm,形态上由规则转为不规则等。
而当动脉瘤生长至直径超过4mm时就要尤其小心,破裂的风险将大大提高。当动脉瘤直径大于7mm,可压迫周围组织或者神经,影响部位不同,症状也不同。较常受到压迫的是动眼神经,表现为单侧眼睑下垂、瞳孔散大、直接和间接光反射消失。
保持稳定,无破裂,无生长:相较稳定而言,破裂与生长均为不稳定。稳定意味着,动脉瘤较小、风险较低,它不会造成压迫症状,也不会破裂造成致命性、灾难性后果。而不稳定意味着,动脉瘤较大、风险较高,它会造成压迫症状,有神经功能障碍,甚至会破裂造成致命性、灾难性后果。
手术入路的选择:ILSA or 颞下入路
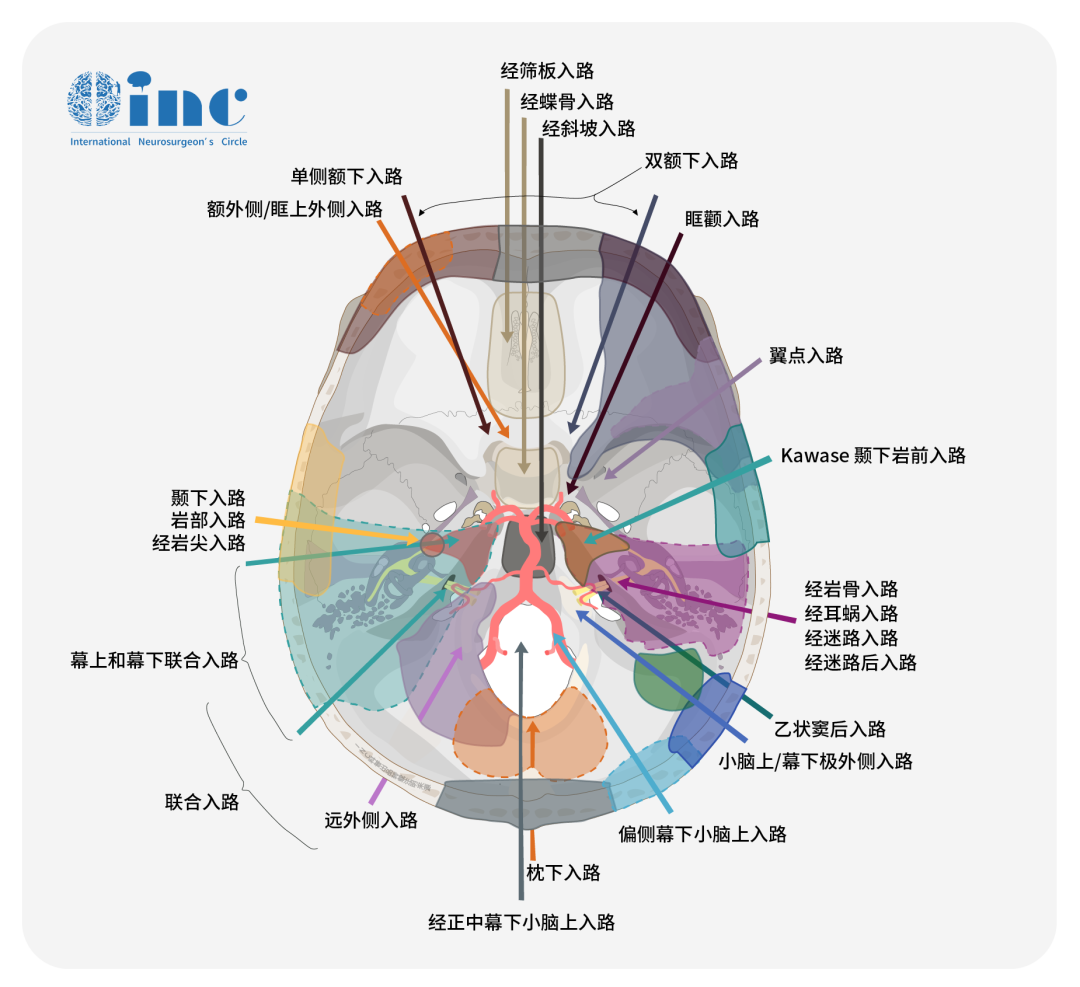
在上述两则案例中,川岛教授均采用颞下入路实施STA-PCA搭桥手术来治疗,而另有学者提出小脑上幕下极外侧入路(ILSA)实施枕动脉(OA)-PCA搭桥手术。对此,川岛教授在研究中也一一进行说明。
有学者建议通过小脑上幕下极外侧入路(ILSA)实行枕动脉(OA)-大脑后动脉(PCA)旁路手术治疗P1/P2动脉瘤。每种方法都有一些优点和缺点,我们想讨论一下。
首先,我们认为通过 ILSA 到 PCA 的手术距离比颞下入路长,通过 ILSA 获得可以操纵搭桥手术的区域也更窄且有限。PCA在幕上运行,因此 ILSA 只能暴露 P2 的后部或 P3 的前部。
尽管颞下入路的主要缺点是回缩时颞叶损伤的风险,然而,通过腰椎引流释放50-100mL的脑脊液、充分暴露和良好的神经麻醉管理可以避免颞叶损伤,这也改善了入路角度。
同时,为了治疗复杂的 P1/P2 动脉瘤,ILSA需要执行额外的手术(血管内技术治疗或其他开颅手术),这会增加并发症的风险。ILSA仅可以暴露 PCA 非常短的部分,并且很难暴露 P2 的近端部分,因此该方法无法实现动脉瘤的近端控制、血栓切除术。
由于在血管内介入期间使用抗凝治疗能够将血栓栓塞的风险降至较低,因此,ILSA这种没有近端控制的远端旁路术增加了术后出血的可能性。而P1/P2 段的血栓形成动脉瘤是远端 PCA 段血运重建的主要适应症之一。
在通过颞下入路放置远端 PCA 旁路时,可以将 P1 到 P3 前部整个暴露出来,这很容易对同一手术区域中动脉瘤的操作。
迄今为止,我们的经验包括1100多例颅外颅内旁路手术,包括 50多例采用OA-PCA搭桥手术。我们的观察表明,OA-PCA不如 STA-PCA是因为它的个体可变性和由于其对周围结缔组织的曲折性、紧密性而导致手术的复杂性。
因此,我们可以预期,使用 OA 移植物的供体血管闭塞风险高于 STA 移植物。因此我们认为,与通过 ILSA 的 OA-PCA 旁路相比,通过颞下入路的 STA-PCA 旁路具有潜在优势。
INC国际动脉瘤手术大师

INC国际神经外科医生集团旗下世界神经外科顾问团(WANG)成员、世界神经外科联合会(WFNS)教育与技术委员会前主席巴特朗菲(Helmut Bertalanffy)教授擅长大脑半球病变、脑干病变、脑血管疾病、脑内深层区胶质瘤、颅颈交界处的病变等的肿瘤切除术、神经吻合术以及各种椎管内肿瘤等。
多年前,巴特朗菲教授及其导师Seeger教授提出了铲平“枕骨髁部”,指出了远外侧入路的关键、操作难度和技术所在,对今远外侧入路的改善和发展奠定举足轻重的作用,是远外侧入路的重要开拓者。这一Bertalanffy版本的经枕髁远外侧入路,仍记载于经典手术专著第6版《施米德克手术学》中。相关案例请看:“潜伏的炸弹”—颅内未破裂动脉瘤,INC国际“拆弹专家”化解危机

INC国际神经外科医生集团旗下组织世界神经外科专家团(WNEG)成员、世界脑血管搭桥手术大师、日本东京女子医科大学神经外科主任川岛明次(Akitsugu Kawashima)教授,擅长脑卒中、烟雾病、颅底肿瘤、面部痉挛/三叉神经痛、颅内血肿、巨大脑动脉瘤、脑动静脉畸形等疾病的治疗,尤其擅长脑血管搭桥、颈内动脉内膜切除术。
神经外科经验:
烟雾病脑血管搭桥手术:1300例
脑动脉瘤夹闭手术:1000例
脑血管畸形切除术:500例
颈内动脉内膜切除术:450例
开颅脑瘤切除术:280例
颅后窝搭桥术、High-flow Bypass技术等

世界知名脑血管搭桥手术专家
国际烟雾病专家
世界知名脑血管搭桥手术专家
日本知名脑血管病手术专家
日本东京女子医科大学八千代医疗中心神经外科主席
日本神经外科学会委员
日本脑卒中协会委员
日本脑卒中外科学会委员
日本急诊医学会委员
参考资料:[1]Kawashima A et. al. Superficial Temporal Artery: Distal Posterior Cerebral Artery Bypass through the Subtemporal Approach: Technical Note and Pilot Surgical Cases. Oper Neurosurg (Hagerstown). 2017 Jun 1;13(3):309-316.
[2]Kawashima, Akitsugu et. al. In Reply: Superficial Temporal Artery: Distal Posterior Cerebral Artery Bypass Through the Subtemporal Approach: Technical Note and Pilot Surgical Cases. Operative neurosurgery (2018).
INC国际神经外科医生集团相关研究
◆栓塞 or 夹闭?动脉瘤还未破裂,INC国际动脉瘤大师将出血扼杀在摇篮中!
◆1/3当场死亡、1/3永久致残?对付动脉瘤破裂出血,也要学会“兵分几路”!
◆“潜伏的炸弹”—颅内未破裂动脉瘤,INC国际“拆弹专家”化解危机

 胶质瘤
胶质瘤 垂体瘤
垂体瘤 脑膜瘤
脑膜瘤 脑血管瘤
脑血管瘤 听神经瘤
听神经瘤 脊索瘤
脊索瘤




 沪公网安备31010902002694号
沪公网安备31010902002694号