尽管在外科和放射技术以及新一代化疗药物方面取得了一些进展,但多形性胶质母细胞瘤(GBM)是较具侵袭性且未分化的脑瘤种,其中位生存期仅为12至18个月。因此,有必要改进目前的治疗方法,并限制与格林-巴利综合征相关的神经症状,如癫痫发作抽搐,这将降低生活质量。这一过程的一步是进一步了解格林-巴利综合征的细胞和分子机制以及潜在的格林-巴利综合征相关癫痫发作,以便设计更精确的靶向治疗策略。胶质瘤抽搐是什么原因?
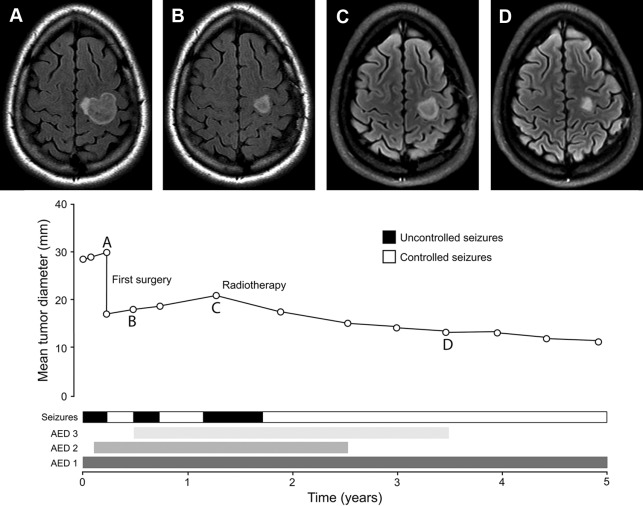
图示:胶质瘤相关癫痫控制情况案例图示
癫痫在弥漫性胶质瘤中很常见,发生在50-90%的低度恶性星形细胞瘤患者和20-50%的胶质母细胞瘤患者中。癫痫发作可能是45%的格林-巴利综合征患者的初始症状,通常是这种致命疾病的一症状。部分性癫痫持续状态是常见的表现,可能与水肿和/或神经炎症有关。虽然癫痫在低级别胶质瘤中更常见,但在高级别胶质瘤中癫痫发作更难控制。
与癫痫相关的格林-巴利综合征是一种复杂的神经障碍。虽然单一癫痫发作可能是格林巴利综合征的一表现,但与格林巴利综合征相关的癫痫发作在频率和严重程度上都变得反复发作。这种继发性癫痫发作的过程涉及到神经元网络的几个分子和细胞重排。与原发性癫痫发作一样,没有药物可以终止继发性癫痫发作过程。虽然一些抗癫痫药物可以降低癫痫发作的频率,提高格林-巴利综合征患者的生存率,但单次癫痫发作可能会加脑发展为癫痫持续状态,并导致其临床并发症。此外,在随访期间,抗癫痫药物毒性对至少25%患者的神经系统发病率有影响,因此恶化了患者的生活质量,并干扰了缺乏放射学证据的临床反应标准评估。因此,我们研究的较终目标是确定肿瘤诱导癫痫发作的分子基础,并开发新的临床模式,其与抗癌治疗平行,将针对癫痫发作。在这里,我们提出了一个新的肿瘤诱导癫痫的假设机制,它可以作为开发早期治疗干预的模板。
Src家族激酶(SFKs)是非受体酪氨酸激酶,介导细胞增殖、分化、侵袭和转移的信号通路。在SFKs中,Fyn和Lyn在中枢神经系统中表达高。我们使用Rembrandt数据库进行的分析显示,与非肿瘤性脑组织相比,胶质母细胞瘤中Lyn上调2倍,Fyn上调1.5倍(P<0.001)。Src表达无明显变化。Kaplan Meier对Lyn和Fyn上调患者的图分析显示,与其他胶质瘤相比,患者的生存率明显更差。其他研究也支持Lyn和Fyn激酶在GBM发病机制中的作用。
中枢神经系统中Lyn和Fyn激酶的高表达,可能与GBM相关的癫痫发生有关。Fyn介导的信号对中枢神经系统和大脑功能的正常发育至关重要。早期的研究只在神经元和少突胶质细胞中表达Fyn,但现在有证据表明Fyn在参与反应性胶质细胞增生的星形胶质细胞中高表达。Fyn在突触可塑性中发挥重要作用,提示Fyn可能参与了癫痫的发生,并可能损害神经元-星形胶质细胞通讯的调节。表达组成性活性Fyn的转基因小鼠表现出增强的兴奋性功能,较高的自发性癫痫发生率和较高的死亡率。另一方面,过表达Fyn的小鼠无明显的癫痫活性。研究还表明Fyn磷酸化NMDA受体亚基NR2A和NR2B,优先磷酸化NR2B。另一项研究使用点燃法和匹罗卡品法建立的大鼠边缘癫痫模型发现,激活含有NR2A但不含nr2b的NMDARs对癫痫的发生是必需的,但两种类型的NMDARs都涉及癫痫诱发的神经细胞死亡。除了Fyn,Src磷酸化NR2A亚基来增强NMDA受体活性。因此,提示NMDA受体NR2A的激活与癫痫发作的发生有很强的正相关关系。
粘连灶激酶(FAK)是一种非受体酪氨酸激酶,在胶质母细胞瘤细胞中上调。活化的FAK与Src家族激酶和其他信号分子结合,激活促进迁移和增殖的信号通路,促进细胞存活、增殖和迁移等。FAK促进脑内移植瘤细胞增殖。在另一项研究中,与对照组小鼠相比,胶质母细胞瘤细胞中FAK表达的特异性下调提高了存活率。在GBM细胞中,另一种局灶性粘附激酶Pyk2的表达被控制,也出现了类似的结果。由于GBM疾病的进展涉及肿瘤细胞和瘤周微环境之间复杂的相互作用,黏附激酶激活的多种信号通路可能有助于肿瘤相关的癫痫发生。
GBM细胞谷氨酰胺合成酶(GS)缺乏可能与癫痫病发生有关。与非致痫性GBM相比,脑瘤标本中GS水平较低,表明GS的下调可能在GBM中起着重要的促痫作用。GS的降低导致肿瘤细胞在瘤周液中积累谷氨酸。神经胶质瘤释放的谷氨酸(Glu)大到足以表明神经氨酸受体的过度激活,激活神经网络导致临床发作。谷氨酸通过Ca2+通透性AMPA谷氨酸受体通过自分泌或旁分泌环在GBM肿瘤的增殖和侵袭中发挥重要作用。AMPA受体在胶质母细胞瘤中高表达,在胶质瘤生物学中发挥重要作用,增强胶质瘤的恶性表型。胶质瘤细胞上的AMPA受体可能调节细胞的运动和肿瘤的侵袭性。通过与Lyn激酶的关联,AMPA受体也可以作为细胞表面信号转导器。通过AMPA受体激活Lyn不依赖于Ca2+,导致MAPK信号通路的激活和脑源性神经营养因子(BDNF)的表达,这可能导致癫痫发作。在另一项研究中,发现在易癫痫的EL小鼠的肥大细胞中Lyn激酶的活性比抗癫痫的ASK小鼠高将近20倍,这表明了Lyn激酶在致痫过程中的作用。此外,有证据表明谷氨酸可以通过EGFR-phospho-akt通路增加GBM细胞EGFR的表达并触发细胞增殖。
Eph受体酪氨酸激酶代表规模较大的受体酪氨酸激酶家族。与正常脑组织[31]相比,高级别胶质瘤中EphA4表达增加。此外,EphA4在细胞中与FGFR1形成复合物,并通过加速FGFR信号通路增强细胞增殖和迁移。Ephrin配体被认为可调节神经胶质相互作用。EphA4的配体Ephrin A3在星形胶质细胞中过表达会增加兴奋性毒性和癫痫的易感性,并降低谷氨酸转运体。EphA4或ephrin-A3的缺乏增加了谷氨酸转运体的丰富度,从而导致谷氨酸的更合适清除。另一方面,胶质谷氨酸转运体的减少增加突触谷氨酸浓度,引起兴奋性毒性,可能导致癫痫和神经退行性变。这些结果表明,epha4介导的信号通路参与了GBM的侵袭性,也为星形胶质细胞调节突触功能和可塑性提供了重要机制。
难治性脑胶质瘤相关癫痫的手术治疗:应用抗癫痫药物过程中出现癫痫复发或加重常提示肿瘤进展(2级证据),脑胶质瘤术后无癫痫发作较长时间后再次出现癫痫发作,可能提示肿瘤复发(2级证据)。脑胶质瘤复发伴频繁的药物难治性癫痫发作时,综合患者情况,可以手术治疗。没有复发的术后脑胶质瘤伴频繁癫痫发作,可按照难治性癫痫进行多方位评价,对于药物难治性脑胶质瘤相关癫痫且明显影响生活质量,可考虑手术(3级证据)。

 胶质瘤
胶质瘤 垂体瘤
垂体瘤 脑膜瘤
脑膜瘤 脑血管瘤
脑血管瘤 听神经瘤
听神经瘤 脊索瘤
脊索瘤




 沪公网安备31010902002694号
沪公网安备31010902002694号