年轻的Z老师,寒窗十余载,终能到大学执教,施展自己的抱负、践行自己的理想,可是近1年来却反复右臂的感觉麻木障碍,有时甚至放射延伸至右半部面部,并出现了语音障碍,单词识别困难,伴有疲劳和精神不振,严重影响了自己的工作。后就诊医院检查发现岛叶占位,考虑岛叶肿瘤引起的反复癫痫发作,当地医生告知患者该位置紧靠功能区,术后发生瘫痪、认知障碍等风险较大,为此Z老师四处求诊,希望能够找到可以有更好的治疗效果,后慕名INC国际神经外科顾问团成员、国际神经外科联合会WFNS教育委员会主席、德国INI国际神经学研究所Helmut Bertalanffy(巴特朗菲)教授,于是联系巴教授,得到了他的病情评估,得知肿瘤可以顺利全切、不会有明显手术并发症,他们终于在黑暗的国际中看到了希望,便咨询至德国INI医院治疗。
手术:左侧翼点入路开颅手术,肿瘤全切手术,使用术中神经导航和术中MRI辅助。一次术中MRI扫描显示大约80-90%的肿瘤已被切除。仅在深岛区域和背侧残留有5-14mm厚度的肿瘤边缘,在术中MR导航设备已使用新的数据集进行了校准。术中MR检查结束,再次消毒铺巾,使用术中导航系统识别肿瘤的其余部分,并通过Cusa逐渐将残存肿瘤切除。显微镜下确认肿瘤全部切除,再次使用术中MR检查并且确认全部肿瘤已经被切除。关颅,手术结束,肿瘤全切历时约3小时,手术顺利。
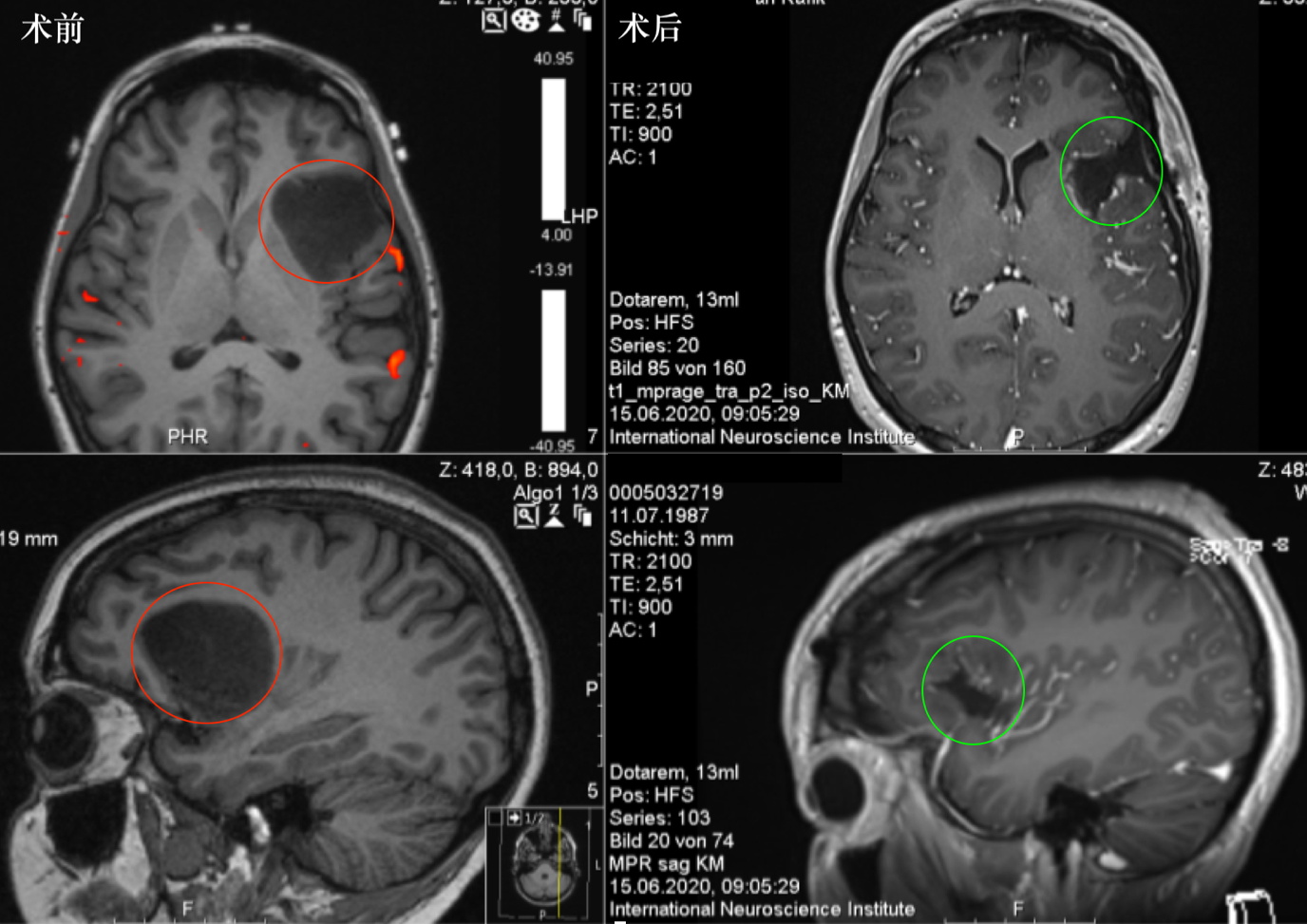
图:术前MR显示岛叶占位,直径约为4 cm,紧邻重要脑功能区,包绕左岛叶的大部分,并在背侧延伸至岛叶的后部。术后MR显示肿瘤全切,无脑出血、水肿等正常脑组织损伤。
术后14天:出院,神志清楚,语言流利,全身状态好,无肢体无力、感觉麻木等问题。
岛叶胶质瘤解读
岛叶是大脑旁边缘系统的一个重要结构。岛叶皮质是旧 皮质和新皮质相连的中间皮质结构,岛叶与整个大脑皮质及皮质下核团均有丰富的神经联系,是个多种功能的汇集区域。岛叶 的功能主要包括内脏感觉、辅助运动、躯体感觉、听觉功能以及 复杂的语言功能,同时协调来自于自身情感意识的内部和外部信息,在经验、情感和行为活动中起平衡作用。
岛叶是神经胶质瘤的好发部位,大约有25%的低级别胶质 瘤及10%的高级别胶质瘤发生在岛叶,大多数岛叶胶质瘤为低级别胶质瘤旧。岛叶在解剖 和功能上并不是孤立的,它是旁边缘系统(岛叶一额眶回一颞 较)的重要;岛叶与其毗邻结构(边缘系统和新皮质)之间不存在 明确的界线,它在这些系统之间起到中转作用,并且在解剖上与 之密切相关。因此,岛盖新皮质、旁边缘系统及边缘系统应被视 为一个复合体。在这个系统内发生的肿瘤,常常以岛叶为中心, 向外延伸生长。岛叶胶质瘤只有少数局限于岛叶皮质内,多数突破环岛沟,侵袭至相应岛盖新皮质,也常常以岛叶为中心扩展至整个边缘和旁边缘系统。在岛叶的前部、钩状束将旁边缘系统的额眶回和颞较相联系,边缘系统和旁边缘系统通过梨形嗅 皮质相联系,而弓状束呈“c”形环绕岛叶,联系额、顶、枕、颞 叶。岛叶的胶质瘤常沿着这些白质纤维束走行方向弥散生 长,多形成指突样复杂的肿瘤。岛叶皮质的内侧紧邻壳核、 苍白球、尾状核及内囊,这些结构的血供来自于大脑中动脉M1 段的分支一豆纹动脉群。岛叶胶质瘤向内侧生长时,压迫内侧结构可造成其移位,更重要的是肿瘤常包绕豆纹动脉群,术 中损伤这些动脉会造成严重的神经功能障碍。岛叶胶质瘤生长 过程引起的主要症状为癫痫,涉及岛叶的癫痫体系包括颞一外 侧裂一岛叶体系、颞一边缘一岛叶体系和内侧额眶一岛叶体 系。

图:岛叶肿瘤范围及术中血管关系。注意外侧豆纹动脉起自M1段,并代表肿瘤切除术的内侧界。M2的短穿支为肿瘤提供血运。M2长穿支有可能穿越肿瘤,但大多数情况为放射冠供血(特别是那些向中央沟走行的),所以术中需被保护(上图)。上下环岛沟为切除术提供了解剖学的上下边界(下图)。暴露环岛沟确定了充分打开外侧裂,确保了残余肿瘤没有隐藏在术者视野的盲点。
鉴于岛叶在解剖关系和功能上的复杂性,岛叶胶质瘤 的外科治疗仍有很大的挑战性。目前多数观点认为,对于各级 别的岛叶胶质瘤,的手术切除都有助于延长患者的生存期。 对于低级别岛叶胶质瘤,扩大切除范围有助于延长无进展生存 期,并有利于开展术后辅助治疗。
手术操作技巧:
1.分离外侧裂
开颅及分离外侧裂时需予患者适量镇静药物。当外侧裂已充分分离,上下环岛沟暴露,肿瘤外侧部经外侧裂入路移除后,方可唤醒患者。
运用“自内向外”(“inside-to-outside”)技术分离外侧裂。首先分离侧裂池远端的较宽处,并逐渐深入外侧裂直至明确岛叶表面的MCA支远端。接着,离断表面的外侧裂蛛网膜。

图.外侧裂前点(anterior Sylvian point)恰位于三角部顶点的下方,其为侧裂池较宽大的部分,可以选做分离外侧裂的起点。笔者一般自远处深部打开外侧裂后,分辨出MCA的远支作为继续分离外侧裂的标志。也就是所谓的“自内而外”(“inside to outside”)、自深向浅、自后向前分离。笔者会避免大家常用的“自外而内”的分离技术,因为由于额颞盖的粘连以及缺乏标志物引导,该分离方法实施较为困难。颞区侧裂浅静脉(superior Sylvian vein)需保护。更多外侧裂分离的细节已在《外侧裂分离技术》一章探讨。
沿M1段远端完成外侧裂分离后,可推移颞盖及额盖从而暴露岛叶。颞盖与岛叶之间存在MCA分支使颞盖比额盖更易活动。偶尔遇到的外侧裂桥静脉可以电凝并离断。近端外侧裂分离应显露M1段远端和LLAs,以此减少术中对岛盖的牵拉。
由于岛盖后部连接紧密,外侧裂远处的分离往往受到限制。此区域的盲目操作可能导致颞上回损伤。用吸引器及双较电凝轻移额颞盖可暴露岛叶皮质与环岛沟。肿瘤常常侵犯岛叶皮层并与岛盖部形成粘连,分离时可能导致肿瘤表面出血,术中可牺牲M2短小表浅的穿支方便止血,使显微手术顺利进行。需避免对出血点盲目的过度电凝。
仅分离外侧裂为切除中等体积到大体积的岛叶肿瘤提供的手术通道相对较窄。另外,M3分支往往连接额颞盖与岛叶上部,进一步限制额叶的移动,使该部分肿瘤难以显露和切除。这些限制是造成岛叶肿瘤次全切除的常见原因。
由于这些肿瘤经常不同程度侵犯颞叶或额叶,所以往往需要额外在额颞盖皮质做切口或切除部分皮质,使其有足够的空间较大限度切除肿瘤。当行额下回及颞上回皮质切口时,有必要对患者面部功能区域(若为非优势半球肿瘤)、Broca区及Wernicke区定位(若为优势半球肿瘤)定位,确保切口部位的顺利。这些操作增加了工作空间及角度,有利于在减少手术盲点的同时充分暴露肿瘤。
在开始切除肿瘤前,确保上下环岛沟充分暴露。
2.岛叶肿瘤切除

图. M2的岛叶皮质穿支需被完全电凝、锐性分离,避免牵拉时损伤上级血管(左图)。上级血管的撕扯伤可导致血管痉挛甚至闭塞,使远部MCA支配区域发生缺血性损伤(右图)。如果术中发现MCA血管壁有轻微损伤,可用凝血酶棉片覆盖破损处,稍加压即可止血。止血后棉片可弃去。罂粟碱浸泡的明胶海绵可缓解操作时M2-M3段血管的痉挛。注意不可盲目电凝止血。
在唤醒患者前,需先行将岛叶外侧部分肿瘤切除。因此,M2短穿支可电凝离断,牵开M2暴露被肿瘤侵犯的岛叶皮质。在不过度牵拉岛盖的情况下较大水平暴露岛叶皮层是重要的。如果肿瘤累及前颞叶区,可行前颞叶局部切除术,以此获得自下而上切除肿瘤的入路。

图. 一旦穿支动脉已电凝离断,可在M2分支间的岛叶皮质做数个软膜切口,从而为软膜下切除肿瘤提供窗口与通道。M2分支的不合理牵拉会损伤这些动脉,影响肿瘤切除范围。

图.囊内减小肿瘤体积(intracapsular debulking)应为手术切除的一步。肿瘤的上下界可按坏岛沟的位置进行估计。肿瘤中心可用双较电凝及吸引器清除。在实施减瘤术时相对保守,病人唤醒并实施皮层下定位与神经功能检测后才着手处理肿瘤边界处。
为了防止MCA损伤,避免使用超声吸引刀,而使用双较电凝和普通吸引器处理肿瘤。将MCA的分支与外侧豆纹动脉保留在视线范围内,防止它们在操作中无意间损伤。
外侧豆纹动脉是可靠的解剖学标志,用来界定可顺利暴露、切除的较内界。它们通常靠内侧走行。尽管上下环岛沟勾勒出了手术区域的上下界,但这些标志常常会受肿瘤生长而发生偏移,故需神经导航进一步指导术者。位于肿瘤后上方走行的M2-M3长穿支血管需严格保护。?
肿瘤外侧部切除后,可唤醒患者,行皮层下定位指导肿瘤上部及后部的切除。

图. 该图示经外侧裂入路行局限于岛叶的肿瘤切除术的切除范围。外侧豆纹动脉(LLAs)组成了该空间的前界和内界。在切除中,LLAs与纹状体(注意它特征性的肉豆蔻样外观)是内界的2个解剖标志。放射冠及内囊后肢位于此空间的后上方的边界处。此处肿瘤的进一步切除需依靠皮层下定位数据及患者直接反馈(术中测试),避免损伤这些白质束。
在皮层下定位技术的帮助下,继续行肿瘤切除术。需要保护LLAs动脉穿支所在区域,而吸引器很容易损伤这些穿支动脉。此内侧区域的任何出血都可使用浸有凝血酶的明胶海绵适当加压止血。
如何判断肿瘤切除的合理深度是个有挑战性的问题,远端LLAs为此提供了一个重要的标志。由于内侧结构受脑偏移的影响较小,故此时神经导航也提供了额外帮助。高度放大、亮度充沛的显微手术视野下,术者依靠其丰富手术经验,观察组织的连续性、颜色、质地的变化,从这些细节中寻找区分肿瘤边界与正常白质的线索。
在内囊后肢处处理肿瘤后界也是该手术较有挑战性的部分之一,在这较后阶段依旧需要耐心运用皮层下定位技术辅助。一旦神经功能出现轻微、可逆的受损,应立即停止操作。
3、术中测试时发现患者出现轻微的神经功能损伤。
术者也需考虑手术时长。一般而言,大多数病人可以配合完成大约3~4小时的清醒状态下手术过程。不使用术中磁共振技术,因为它会使患者清醒阶段的手术时间延长。
岛叶胶质瘤治疗进展.中华神经外科杂志.

 胶质瘤
胶质瘤 垂体瘤
垂体瘤 脑膜瘤
脑膜瘤 脑血管瘤
脑血管瘤 听神经瘤
听神经瘤 脊索瘤
脊索瘤




 沪公网安备31010902002694号
沪公网安备31010902002694号