松果体区可出现多种肿瘤组织学,包括实质性肿瘤、神经外胚层肿瘤、生殖细胞肿瘤和脑膜肿瘤。松果体区的胶质瘤包括纤维状星形细胞瘤、毛细胞性星形细胞瘤、间变性星形细胞瘤、胶质母细胞瘤、少突胶质瘤、室管膜瘤和脉络丛乳头状瘤。多形性胶质母细胞瘤(GBM)在松果体区少见。本文报告一例松果体区原发性GBM病例,讨论其临床过程、影像学表现及治疗方法。
病史摘要:
一名64岁男性,无明显既往病史,表现为垂直复视,头痛3周,失眠6个月。他的神经检查显示右颅神经四型麻痹和步态困难。在一次出现后1个月,随后的CT成像显示松果体区有一个边缘不良的高密度肿块。胸部、腹部和骨盆的计算机断层扫描和整个脊柱的核磁共振成像显示没有转移疾病的证据。大脑的核磁共振成像显示了一个不均匀增强的松果体块,大小为2.3厘米× 2.5厘米× 2.3厘米(图1)。由于其位置,病变被认为是不可切除的,并进行图像引导立体定向针活检。病理显示一个由明显非典型细胞组成的高级别神经胶质瘤,许多细胞具有较大的细胞核,并含有丰富的有丝分裂活性(三个高能量场中的七个有丝分裂)、多个微血管增生病灶和假凋亡坏死区域,符合GBM,国际卫生组织四级(图2)。肿瘤呈阳性O-6-甲基鸟嘌呤-DNA甲基转移酶(MGMT)甲基化,异柠檬酸脱氢酶1/2突变阴性。患者的GBM采用同步放化疗,随后辅助化疗。患者接受调强放射治疗,剂量为60戈瑞,每日2戈瑞,同时给予替莫唑胺75毫克/米2。初始场的剂量为50 Gy,包括沿增强肿瘤和周围水肿的白质束2厘米的边缘,还覆盖临床目标体积中的三和四脑室、侧脑室、脑导水管、顶盖、部分丘脑和部分脑干。大部分侧脑室被覆盖,但由于担心额外的毒性,角的较末端被排除在外,考虑到所治疗的脑体积,优势池不是特别针对的。根据先前描述松果体区GBMs软脑膜疾病传播倾向的临床报告,努力覆盖大部分脑室。在较初的放射治疗计划后,对沿白质束边缘2厘米的增强肿瘤增加10戈瑞。组合放射治疗计划如图所示图3。患者在放射治疗过程中使用了地塞米松,因为担心放射治疗可能会加重局部水肿,从而导致脑导水管阻塞。
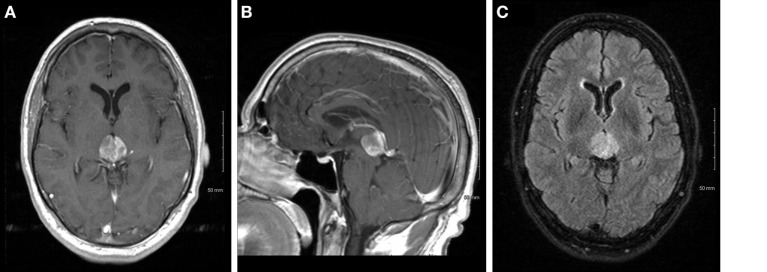
图1:轴位(A)和矢状位(B) T1造影后和T2液体衰减反转恢复(C)肿瘤较初表现的图像。
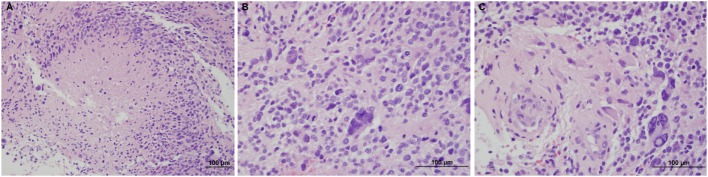
图2:苏木精、伊红染色,20×(A)呈坏死,40×(B)有丝分裂,40×(C)微血管增生。
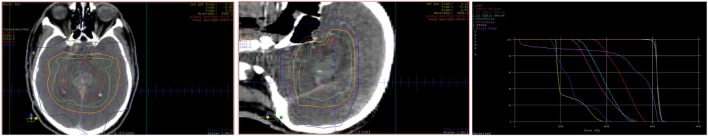
图3:放射治疗计划剂量分布的轴向和矢状视图,带有剂量-体积直方图。
患者在放化疗过程中出现脱发和不良事件通用术语标准4版1级皮炎,但在其他方面对同步放化疗耐受性良好。每天的计算机断层扫描用于放射治疗图像指导,并且在治疗期间没有显示脑积水发展的迹象。放射治疗完成后4周的磁共振成像显示松果体GBM的大小略有减小,为2.3厘米× 2.0厘米× 1.9厘米。他继续用替莫唑胺进行维持治疗,每周期每28天进行5天,剂量为150毫克/米2并增加到200毫克/米2用于后续循环。
活检后58周进行了磁共振成像,显示脑干和顶叶有两个新的病变,都在以前的放射治疗范围内。全脊柱磁共振成像没有显示任何液滴转移,也没有任何腰椎穿刺脑脊液播散的迹象。贝伐单抗每3周添加7.5毫克/千克至替莫唑胺疗法(<https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5466962/>)。替莫唑胺在活检后总共88周的17个周期后停用。由于步态障碍恶化的临床症状,对应于放射治疗区内疑似梗死的磁共振成像结果,在活检后129周,贝伐单抗停止使用,随后每2个月进行一次系列磁共振成像,以密切监测他的疾病。在一次活检后146周进行的磁共振成像,与活检后111周开始的多项先前研究进行比较,显示松果体肿块的大小从11毫米× 11毫米细微地逐渐增加到14毫米× 11毫米,融合的脑室周围白质T2/液体减弱了非特异性和稳定的反转恢复高强度,这在活检后166周的磁共振成像中得到再次证实(图4)。
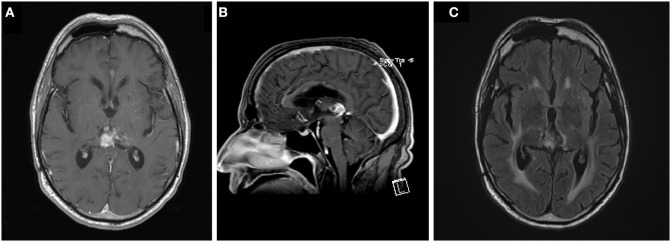
图4:轴位(A)和矢状位(B) T1造影后和T2液体衰减反转恢复(C)肿瘤在开始放化疗166周后的较终随访图像。
临床上,患者仍有复视,可通过棱镜眼镜矫正。复视继续导致步态障碍,这已经通过物理治疗得到好转,患者不再需要使用拐杖。较后一次见到他是在活检后166周和化疗开始后156周。他一直受到严密的监视,不接受全身治疗。
松果体GBM是一种少见的疾病,预后不良。大多数患者出现颅内压升高的迹象和视觉症状。很难从几十年来不同治疗模式下报告的少数患者总数中得出结论。这是一个报道阳性MGMT启动子甲基化和贝伐单抗在进展中使用的松果体区GBM。我们的病例表明,在没有完全手术切除的情况下,可以潜在地实现对疾病的持久控制。需要进一步研究MGMT甲基化作为预后指标的作用以及松果体区GBM对贝伐单抗的反应。

 胶质瘤
胶质瘤 垂体瘤
垂体瘤 脑膜瘤
脑膜瘤 脑血管瘤
脑血管瘤 听神经瘤
听神经瘤 脊索瘤
脊索瘤




 沪公网安备31010902002694号
沪公网安备31010902002694号