胶质母细胞瘤(Glioblastoma,GBM)是常见的原发性恶性脑瘤,占全部原发性脑和中枢神经系统肿瘤的16%(Thakkar et al.,2014)。年龄调整后的平均发病率为3.2/10万人(Ostrom et al.,2015;Ostrom,Gittleman等,2014)。虽然GBM几乎只出现在大脑中,但它们也可以出现在脑干、小脑和脊髓中。61%的原发性胶质瘤发生在大脑的四个叶:额叶(25%)、颞叶(20%)、顶叶(13%)和枕叶(3%)(美国神经科学护士协会[AANN],2014)。较初,GBM被认为仅仅来源于胶质细胞;然而,证据表明,它们可能来自具有神经干细胞样特性的多种细胞类型。这些细胞处于从干细胞到神经元再到胶质细胞的分化的多个阶段,表型变异很大水平上取决于信号通路的分子改变,而不是细胞来源的不同(Phillips et al.,2006)。
GBM平均年龄为64岁(Thakkar et al.,2014),但可能发生在任何年龄,包括儿童。男性的发病率略高于女性(1.6:1),白种人的发病率相对于其他种族(Ellor,Pagano-Young,&Avgeropoulos,2014)。GBM可以分为初级的或从头开始的,没有已知的前身;或者是继发性的,随着时间的推移,低级别肿瘤转变为GBM。大多数GBM是原发性GBM,这些患者往往年龄较大,与继发性GBM患者相比预后较差(Wilson,Karajannis,&Harter,2014)。
胶质母细胞瘤四级原因:风险因素
在查明这种疾病与环境和职业接触的具体联系方面的努力基本上是不确定的,也力度不足。电离辐射是少数已知的能明确显示胶质瘤发展风险增加的危险因素之一(Ellor et al.,2014)。辐射诱导的GBM通常是在其他肿瘤或疾病的治疗性放疗后数年才出现(Johnson et al.,2015)。其他环境暴露于氯乙烯、杀虫剂、吸烟、石油精炼和合成橡胶制造与胶质瘤的发展有着松散的联系。电磁场、甲醛和手机的非电离辐射尚未被证明会导致GBM(Alifieris&Trafalis,2015)。神经胶质瘤发展的风险增加见于一些特定的遗传疾病,如神经纤维瘤病1和2、结节性硬化症、李-弗罗梅尼综合征、视网膜母细胞瘤和特考特综合征;然而,不到1%的胶质瘤患者有已知的遗传疾病(Ellor et al.,2014)。
胶质母细胞瘤四级临床表现
新诊断的GBM患者的表现可能因肿瘤的大小和位置以及受累大脑的解剖结构而有很大差异(Lobera,2015;Young等,2015)。患者常表现为颅内压升高的症状,包括头痛和局灶性或进行性神经功能障碍。癫痫发作是多达25%的患者的主要症状,可发生在多达50%的患者的疾病晚期(Perry et al.,2006;希夫等,2015)。目前对癫痫发作患者的护理标准包括使用抗癫痫药物(AEDs),但不建议对无癫痫发作的患者常规使用AEDs(Glantz et al.,2000;佩里等人,2006年)。许多患者在诊断时被开皮质类固醇,以帮助控制血管源性水肿和减轻伴随的体征和症状。
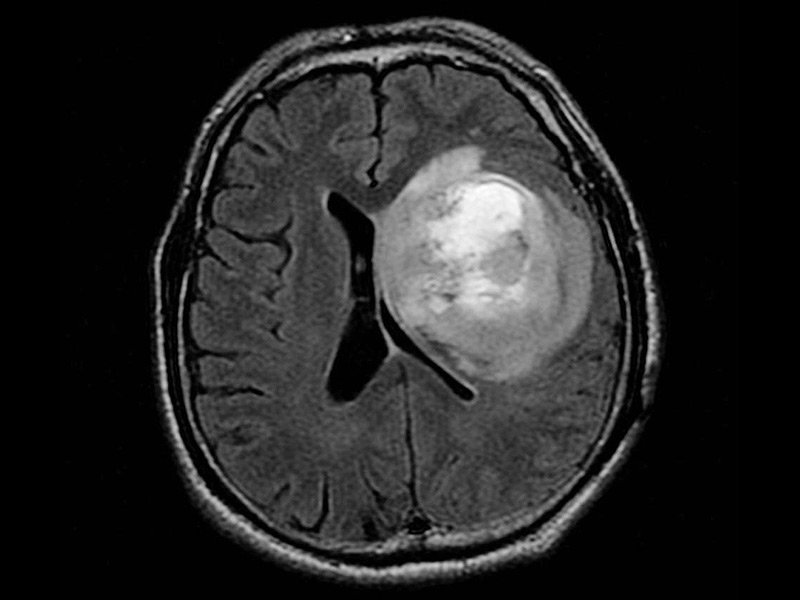
初始诊断成像可能包括计算机断层扫描(CT)或磁共振成像(MRI)扫描。在MRI上,几乎全部的GBM在钆造影剂下增强,表现为不规则形状的肿块,致密的强化环和低密度的坏死中心。坏死是GBM的标志性特征,坏死的存在是脑瘤在国际卫生组织分类体系中被划分为四级或GBM的必要条件(AANN,2014)。诊断影像学上也可能出现周围血管源性水肿(可能导致肿块效应)、出血和心室扭曲或移位(Ellor等,2014;Johnson等,2015)。
在约13%的病例中,GBM可表现为多灶性(大于两个病灶,包括软脑膜扩散)、远端性(二病灶与原发病灶不相邻)或弥漫性疾病,并且已经证实,显微镜下肿瘤浸润通常超过MRI上可见的信号异常(Chamberlain,2011;Johnson等,2015)。
胶质母细胞瘤四级治疗
新诊断的GBM的治疗需要多学科的方法。目前的标准治疗包括较大限度的顺利手术切除,同时给予口服烷基化化疗药物替莫唑胺(TMZ)(Temodar®)放疗,然后给予TMZ辅助化疗(National Comprehensive Cancer Network[NCCN],2015)。广泛而完整的手术切除GBM是困难的,因为这些肿瘤通常是侵袭性的,并且通常位于大脑的重要区域,包括控制语言、运动功能和感觉的区域。由于原发肿瘤肿块侵袭性高,根治性切除不能治愈,浸润性肿瘤细胞始终停留在脑周围,导致后期疾病进展或复发(Wilson et al.,2014)。
多项研究表明,在可能的情况下的手术切除是很重要的,切除范围更大的患者预后更好(Kuhnt等,2011;Roder等,2014)。在一些研究中发现,更大范围的切除与更长的无进展生存期(PFS)和总生存期(OS)之间存在有统计学意义的关联(Keles,Anderson,&Berger,1999;Lacroix等人,2001年;Mukherjee&quinnes-hinojosa,2011年;(Stummer等,2006)。手术和术前定位技术的改进使得在保持功能和生活质量的同时实现更广泛的切除成为可能(Mukherjee&Quinones-Hinojosa,2011)。
在术前计划中使用功能性MRI和弥散张量成像(DTI),以及在手术中使用超声、CT扫描和MRI直接刺激,使得多模态神经导航和患者特定解剖和功能数据的集成成为可能。尽管有这些技术,区分正常大脑和残余肿瘤仍然是一个挑战,使用5-氨基乙酰丙酸(5-ALA)染料进行荧光引导已被发现比传统的神经导航引导手术更合适(Zhao et al.,2013)。然而,一项Cochrane综述发现,使用5-ALA、术中MRI或DTI神经导航的图像引导手术增加了高级别胶质瘤患者术后MRI完全切除肿瘤的比例(Barone,Lawrie,&Hart,2014)。这些新技术的其他限制包括成本和对专门设备、操作人员和手术套件的需要。在将其作为全部GBM患者的治疗标准之前,还需要进一步的研究来明确其临床益处。
即使在手术切除方面取得了进展,GBM患者的预后仍然很差,中位生存期为15个月(Thakkar et al.,2014)。除了手术切除范围外,其他因素也与OS的增加有关。患者的年龄和Karnofsky性能状况被广泛认为是预后因素,年龄越低、性能状况越好,患者的生存期越长。大于5-6cm的肿瘤和那些越过中线的肿瘤与阴性结果相关(Ellor et al.,2014)。幕上(大脑)和小脑肿瘤比脑干或间脑肿瘤更易于手术治疗,预后更好(Walid,2008)。Johnson和O'Neill(2012)的一项分析表明,自的多模式治疗开始以来,OS在统计学上有好转。
胶质母细胞瘤四级复发
尽管较大限度的初始切除和多种治疗,约70%的GBM患者在诊断后一年内会出现疾病进展(Stupp et al.,2005),只有不到5%的患者在诊断后存活5年(Ostrom,Bauchet,et al.,2014)。对一些患者来说,再切除是一种选择,手术减积可以减轻复发时常见的肿块效应和症状,如癫痫、语言障碍和运动障碍。重复手术可能需要确认肿瘤复发、假性进展或放射性坏死的诊断,也可能提供组织分子测试,以确定潜在的新的靶向药物(Brandes,Bartolotti,&Francheschi,2013)。对于重复手术是否能增强OS,意见不一。有证据表明,复发时更大范围的切除可提高生存率(Bloch et al.,2012;McGirt等,2009年);然而,其他研究没有发现在生存方面的益处(Brandes et al.,2013;Franceschi等,2015)。
一些患者可能会接受额外的辐射,但健康脑组织对辐射的耐受性有限,因为辐射坏死的风险增加了。各种各样的放射技术,包括近距离放射治疗、伽玛刀和立体定向放射外科,可用于复发性疾病的治疗(Davis&Stoiber,2011)。
GBM复发时,化疗和皮质类固醇可用于缓解症状和好转生活质量,但客观缓解率低,标准细胞毒性药物的进展时间只有3-6个月(Franceschi et al.,2009)。再挑战TMZ可能是一种选择,其他药物,如卡铂(Paraplatin®)、依托泊苷(osar®)、伊立替康(Camptosar®)和亚硝基化疗,可以尝试作为单一药物或方案。贝伐珠单抗(Avastin®)是一种人源化单克隆抗体,以血管内皮生长因子为靶点,该生长因子是血管生成所必需的蛋白质。它在2009年被批准用于复发性GBM疾病。试验已经证明了优越的PFS;然而,操作系统还没有出现有意义的改进(Cohen,Shen,Keegan,&Pazdur,2009)。贝伐珠单抗也被证明可以减少血管通透性和水肿,好转氧合,减少放射性坏死(Niyazi等,2016)。然而,它可能导致潜在的生命危险事件,如出血、血凝块和肠穿孔(Salacz,Watson,&Schomas,2011;Taal等,2014)。
2011年,Optune较初被FDA批准用于复发性GBM的单一治疗。Optune是在接受化疗后经组织学或放射学证实的脑幕上区域复发后出现的,它是GBM在手术和放射治疗方案失效后的标准药物治疗的替代方案(Novocure,2016)。一项随机临床试验表明,与标准化疗相比,生存率相当,副作用更少,胃肠道、血液和感染性不良事件明显更少(Stupp et al.,2012)。该装置没有明显的副作用,主要是阵列(电较)对头皮的刺激,这使得ttfield成为一个有吸引力的治疗选择。此外,患者报告说,与接受化疗的患者相比,认知和情感功能等生活质量指标有所好转。使用Optune交付ttfield已被纳入周期性GBM的NCCN指南(Davis,2013;会发现,2015)。对于复发性疾病的维持治疗,TTFields仍然是一个令人信服的治疗选择。
支持性护理
GBM是一种侵袭性较强的肿瘤,伴随一系列与潜在疾病和治疗相关的并发症。认识和管理这些症状是必要的优化生活质量。许多与治疗相关的副作用(如化疗引起的骨髓控制、恶心、疲劳、便秘)和早期辐射相关效应(如脱发、读写困难、厌食症)并非GBM人群独有,一般可以通过医学手段加以控制。
结论
对于胶质母细胞瘤,为了好转预后,合适的症状管理、注重好转生活质量以及新的治疗方法可能为GBM患者及其家人带来新的希望。
资料来源:ONS publications

 胶质瘤
胶质瘤 垂体瘤
垂体瘤 脑膜瘤
脑膜瘤 脑血管瘤
脑血管瘤 听神经瘤
听神经瘤 脊索瘤
脊索瘤




 沪公网安备31010902002694号
沪公网安备31010902002694号