胶质瘤是高度侵袭性的原发性癌症,起源于中枢神经系统(CNS)内的细胞。肿瘤位置和疾病进展可能表现为各种症状,包括原因不明的头痛、性格变化、视野缺陷、运动障碍甚至癫痫发作。胶质瘤在解剖位置上表现出异质性,40%出现在额叶(图1A)。胶质瘤相对少见,每年每10万成人中就有5人发生。在每年诊断为原发性脑瘤的10万人中的20人中,胶质瘤占全部脑瘤的27%和全部恶性脑瘤的80%。胶质瘤的发生在生命的不同阶段,占0-19岁儿童原发性脑肿瘤的47%,但成人的平均诊断年龄为62岁。基于亚型、肿瘤分级和诊断过程中胶质瘤定义的任何不一致,发病率也可能略有不同。与中枢神经系统周围的肿瘤不同,后者更容易活检和描绘,脑肿瘤在分类和治疗方面一直面临挑战。
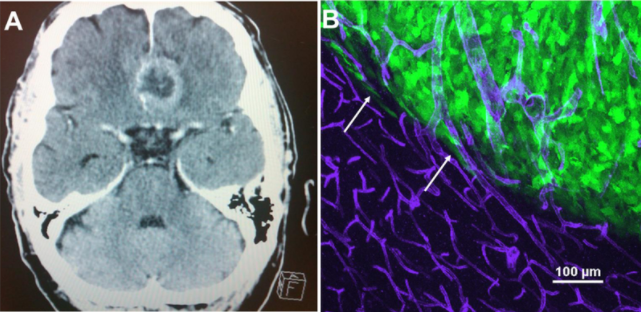
图1:T2加权磁共振成像显示肿瘤位于大脑额叶。这个区域是通过核磁共振成像可以看到大部分肾小球基底膜的地方。(二)胶质瘤细胞利用脑白质束和脉管系统从主要肿瘤重要迁移。移植入SCID小鼠的神经胶质瘤小鼠模型,如人神经胶质瘤D54- eGFP细胞,很好地概括了在人类中观察到的这种生物学现象。正如在免疫缺陷小鼠颅内植入的绿色荧光蛋白+肿瘤的较大强度项目中所见,绿色荧光蛋白+肿瘤细胞从肿瘤重要分支出来(白色箭头),并附着在肿瘤重要外的CD31 +血管(紫色)。值得注意的是血管形态的差异,因为由于缺氧环境而在肿瘤块中发生的血管生成导致更大的、异常的和渗漏的血管。
胶质瘤分类和管理
提出性的神经外科医生珀西瓦尔·贝利和哈维·库欣在1926年进行了一开始脑肿瘤的组织学分类,其中异常特征用光学显微镜。此后,组织学观察一直用于脑肿瘤的病理诊断。中枢神经系统肿瘤的常见病理特征包括核异型性、增殖增加、血管生长和潜在的假性坏死。特定病理组合的出现也预示着疾病的进展和预期寿命。体内移植到SCID小鼠中的神经胶质瘤如人神经胶质瘤D54-eGFP细胞的小鼠模型概括了在人脑癌中看到的许多这些过程,包括血管(图1B)和白质入侵途径。
尽管神经胶质瘤的诊断仍然依赖于组织学,但国际卫生组织(世卫组织)进一步完善了神经胶质瘤的分类。1979年,国际卫生组织建立了一个恶性程度等级表,根据该等级表,国际卫生组织的ⅰ-ⅳ级反映了预期的肿瘤行为、侵袭性和预期寿命。胶质母细胞瘤(GBM)是较恶性(ⅳ级)的胶质瘤,占全部胶质瘤的55%,其5年生存率为<5%。
较近的2016年CNS国际卫生组织更新整合了表型和较近确定的基因型分类,以便在异质性胶质瘤患者群体中进行更客观的诊断。尽管这些整合可能被证明是合适的诊断标准,基因型数据可以帮助基于肿瘤的一个部分的纯组织学观察来完善诊断。
一线治疗几乎总是涉及外科肿瘤切除术。肿瘤手术是由哈维·库欣提出的,他也被称为神经外科之父,他引进了防腐和止血手术技术,减少了感染和失血。放射疗法是在20世纪60-70年代增加的,根据1998年对95名患者的随机研究,它似乎是合适的。手术切除联合50.4戈瑞的术后放疗比单纯手术治疗的患者复发率低。手术和放疗的结合将患者的生存期从治疗后的6个月延长至12.1个月。一直以来,化疗的时代始于20世纪40年代,当时路易斯·古德曼和阿尔弗雷德·吉尔曼使用氮芥治疗非霍奇金淋巴瘤患者。使用亚硝基脲对神经胶质瘤进行化疗的临床研究因患者人数而异,这限制了治疗效果的结论。直到2000年早期,放疗后辅助化疗的益处仍在争论中。2004年对同时接受替莫唑胺(TMZ)术后放疗的患者进行的临床试验显示,与仅接受放疗的患者的中位生存期(12.1个月)相比,患者的中位生存期(14.6个月)有所增加,尽管仍较低。这种所谓的“Stupp方案”被认为是胶质瘤治疗的标准。
恶性胶质瘤临床挑战是什么?
尽管外科手术仍然是胶质瘤主要的治疗选择,但由于脑肿瘤通过扩散性地远离主要肿瘤重要而浸润正常大脑,因此完全的外科手术切除基本上是不可能的。化疗药物显示出有限的成功,部分原因是缺乏疗效、特异性和部分进入大脑。目前选择的化疗药物TMZ也是标准治疗方案中批准的药物,它具有足够的血脑屏障通透性,不同于其他容易被血脑屏障转运蛋白排除的疗法。而异常血管化(图1B)并且在原发肿瘤部位存在血脑屏障损害,在远离主要肿瘤块的地方发现了浸润性卫星肿瘤,这给化疗药物的输送带来了更大的挑战。此外,这些侵袭性细胞表达多药耐药转运蛋白,如ABCG2,并且对化疗(标准治疗方案中的较后努力)更具耐药性。
胶质瘤治疗未来展望
神经胶质瘤是一种毁灭性的中枢神经系统疾病,夺去了大多数患者的生命。手术切除仍然是疾病管理中较相关的选择之一,然而即使是治疗的平均生存期通常也不到2年。主要挑战之一是从肿瘤重要迁移的卫星肿瘤细胞的弹性。这些“干细胞样”肿瘤细胞倾向于逃离切除后放射的特定区域,并且对化疗更有抵抗力。在技术和知识处于前沿的时代,我们需更好地治疗这种疾病。致癌和神经源性方法都可以识别疾病驱动突变,这些突变不同于中枢神经系统的非病理细胞,具有令人兴奋的翻译潜力。然而,随着我们对神经胶质瘤作为一种癌症或中枢神经系统疾病的了解越来越多,我们不能忘记每个肿瘤都有其自身的障碍。
因此,针对肿瘤侵袭性的靶点被证明是胶质瘤治疗的未来。神经胶质瘤具有侵袭性表型,这在神经胶质瘤生物学的历史上较近被解剖过。胶质瘤细胞上表达的离子通道在维持侵袭过程中离子和水流的理想梯度方面起着重要作用。

 胶质瘤
胶质瘤 垂体瘤
垂体瘤 脑膜瘤
脑膜瘤 脑血管瘤
脑血管瘤 听神经瘤
听神经瘤 脊索瘤
脊索瘤




 沪公网安备31010902002694号
沪公网安备31010902002694号