脑海绵状血管瘤又称CM。该病可为散发性,也可为家族性。在这类患者,连续MRI检查发现过新发病灶。脑活检后和放射外科治疗后新发CM,证实病变具有进展特性。
家族性CM和约一半的多发性CM散发病例是由CCM1(KRIT1)、CCM2(MGC4607)和CCM3(PDCD10)致病突变引起。在西班牙语裔美国人中,几乎全部家族性脑部CM病例都与KRIT1始祖突变有关。而在非西班牙语裔白人中,家族性病例与MGC4607和PDCD10有关。
肉眼检查时,CM表现为饱满的成簇紫色颗粒,呈特征性的“桑葚样”外观。其直径为2mm至数厘米不等。显微镜下,CM由扩张的薄壁毛细血管构成,有单层内皮细胞衬附和一层薄的纤维外膜。血管壁中没有弹力纤维和平滑肌。在典型CM中,病灶的血管之间并没有脑组织填充。但这可能不是判定CM的必要标准,因为一项纳入71例CM患者的组织病理学研究发现,50例(70%)患者有脑实质填充,且其他研究也是在部分病例中发现有填充的脑组织。
由于之前的出血,病灶紧邻的周围组织通常会有胶质瘢痕和含铁血黄素沉积。其中包括扩张的毛细血管,可能表明有毛细血管扩张;该发现支持一种整合的观点,即毛细血管扩张和CM分别为CM病程进展的两种结局。在CM病灶中(通常是较大的病灶),可能发现炎症和钙化,偶尔还可发现骨化。
DVA(发育性静脉异常)可合并发生CM。
●一项纳入102例患者的病例系列研究显示,23%的患者有DVA合并CM;相比幕上病灶,颅后窝病灶更常见DVA合并CM。
●随后一项纳入57例CM患者的病例系列研究发现,25%的患者合并DVA,另有35%的患者存在非典型静脉回流伴CM。
大脑是较常见的CM病变部位(70%-90%)。整个幕上区都报道过CM,但较常发生于皮质下,易发于rolandic区和颞区。大多数大型病例系列研究显示,约25%的CM病灶位于颅后窝,其中大部分位于脑桥和小脑半球。脊髓CM为髓内病变,主要见于颈段和胸段。
临床表现和自然病程
CM的男女发病率相同,平均发病年龄为30-40岁,但女性更常发生出血和神经功能障碍。与不伴静脉异常的CM相比,合并DVA或非典型静脉回流的CM更可能出现症状性出血。CM的表现与其所在部位有关。
●幕上CM常表现为出血、癫痫发作和进行性神经功能障碍。数项大型病例系列研究报道,每年的出血率为0.25%-1.1%。癫痫发作和进行性神经功能障碍的原因可能是占位效应和继发性微循环血供不足,或者是微小出血伴局部含铁血黄素沉积,后者可刺激皮质或皮质下组织。
●幕下CM常表现为出血和进行性神经功能障碍。脑干病变表现为颅神经病和长束征,由于该区域有大量重要神经核团和纤维束,可出现进行性神经功能减退。因此,脑干病变的自然病程比其他部位病变更差。脑干病变的出血率为每年2%-3%,再次出血率可达17%-21%。39%的患者可见进行性神经功能减退。
无症状CM的自然病程明显不同于有临床影响的CM。一项纳入122例患者(平均年龄37岁,范围为4-82岁)的前瞻性研究发现,50%的患者较初并无症状。平均随访34个月发现,无症状患者和有症状患者的出血率分别为0.6%和4.5%。在另一队列中,一次出血的5年风险为2.4%,而再次出血的5年风险为29%。出血复发的风险会逐渐下降。
脑海绵状血管瘤诊断
尽管研究一致显示先前出血是后续再次出血的危险因素,但关于出血和神经功能障碍的其他危险因素的研究结果并不一致,包括性别、病灶大小、部位、正在妊娠和多发病灶。至少有一项随访4年的观察性研究提示,抗血栓治疗及口服抗凝治疗并不会影响CM相关出血风险。
诊断—流经CM的血流很少。因此,血管造影可能无法观察到病变,常被称为“血管造影隐匿性”。其他影像学检查对诊断更为重要,是MRI。
MRI
MRI通常能确诊CM。成像方法应包括GRE或SWI,这些技术可能检出常规MRI序列无法发现的较小CM。T1和T2加权像上的特征性表现包括“爆米花”样混杂信号,符合不断演变的血液降解产物的表现(影像4)。出现深色含铁血黄素环提示陈旧性出血,这种环在病灶周围的T2加权像或GRE序列中显示效果较佳(影像5)。MRI上类似于CM的病变包括低级别胶质瘤、出血性转移瘤(如黑素瘤、肾细胞癌)和多形性黄色星形细胞瘤。
一旦发现CM,就应行对比增强影像学检查,以显示出全部潜在的伴随DVA。对比增强和SWI序列常可显示DVA,因其血流正常。另一方面,CM可能有散在的增强信号,强度不一且没有意义。这对手术规划重要,因为切除DVA可能损害正常的皮质静脉回流,从而导致静脉梗死。
CT
CT通常可见不同钙化程度的非特异性、不规则高密度团块。给予造影剂后病灶周围的微弱显像是一种可变的非特异性表现。
血管造影
一般不用导管血管造影来检测CM,除非考虑有AVM。约10%的CM患者可见毛细血管显影或早期回流静脉。这些表现可能类似于脑膜瘤的血管造影表现。
脑海绵状血管瘤治疗
任何部位的无症状CM都可予以观察。对于可探及的症状性大脑和小脑CM,手术切除的指征包括存在进行性神经功能障碍、顽固性癫痫和复发性出血。
●一个研究组报道,经平均1年的随访,65例大脑和小脑CM患者中有97%获得了较好或良好的手术结局。1.5%的患者结局较差,总体死亡率为1.5%。
●一项病例系列研究纳入了168例CM导致症状性癫痫的患者,发现超过2/3的患者在术后3年时无癫痫发作。良好结局的评估因素包括:病变位于内侧颞叶、病变直径<1.5cm以及没有继发性多方位性癫痫发作。
●另一项病例系列研究发现,术前癫痫发作病史较长和术前癫痫发作控制较差是不良预后的评估因素。
手术不可探及的病变
对于病灶完全被重要脑组织(如rolandic区皮质、脑干、丘脑/基底节)包绕的症状性CM患者,尽管未治疗的脑干和丘脑病变自然病程较差,通常仍予以观察处理。
对于这种手术不可探及的病变,立体定向放射外科治疗也许能替代保守治疗,现有证据表明该疗法的确可减少出血,是在放射外科治疗后2年或更长时间。然而,临床经验和现有病例系列研究显示的高并发症发生率使许多人放弃使用立体定向放射外科治疗CM。
例如,一项纳入95例患者共98处病变的回顾性分析发现,在立体定向放射外科治疗后2年的潜伏期后,年出血率从17%降至5%。但在平均随访5.4年时,长期性神经功能障碍的发生率和死亡率分别为16%和3%,且这些并发症是由放射诱导性损伤所致。而且在随访期间,放射相关损伤和病变临床进展的联合效应导致了神经系统功能减退。
根据现有资料,我们建议不使用立体定向放射外科来治疗CM。
这些脑干病变可以手术
如果脑干CM病灶靠近软脑膜表面或病灶中的脑组织,则无论有没有复发性出血,出现进行性神经功能减退时常常给予治疗,因为脑干CM具有侵袭性自然病程。一项关于手术切除脑干CM的系统评价纳入1390例患者,发现45%的患者出现了早期神经系统并发症,84%获得了长期好转,16%病情恶化。一些医疗中心还成功运用了显微外科技术。
脑干海绵状血管瘤案例一则
L女士,年龄45岁,发病2年前发现脑干海绵状血管瘤,偶发小量脑干出血,10天前迅速出现感觉运动障碍,吞咽困难,构音障碍,呼吸功能不全
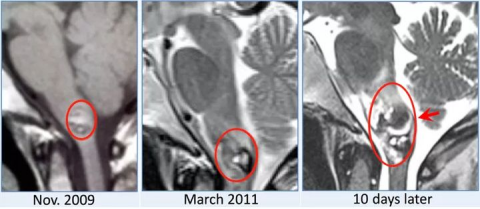
图1:术前MR,2009年发现脑干延髓脑桥海绵状血管瘤,2年后在10天内迅速恶化发生脑干出血。
手术医生
德国INI国际神经学研究所Helmut Bertalanffy教授及其手术团队
手术地点
德国汉诺威国际神经科学中心INI
手术过程
半坐位,显微镜下经膜髓帆入路全切病变,全切除时间为2.5小时,手术顺利

【经膜髓帆入路示意图,利用自然的界面,对组织的损害较小;不仅可以处理四脑室外侧孔内(Luschka孔)的病变,可以磨除C1后弓获得自下而上更为舒适的操作角度,扩大了对脑室侧方的显露】
术后情况
术后1天:ICU治疗观察。术后7天:患者呼吸功能好转,自主呼吸好,无吞咽困难等,遂转到普通病房治疗,患者能在协助下下床、少量活动,在康复师指导下进行康复锻炼。
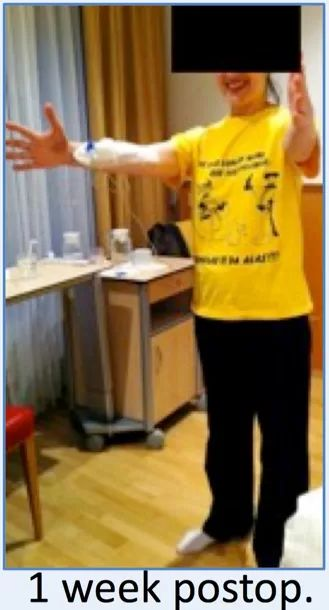
脑干病变成功全切,术后重生,患者从靠呼吸机辅助“躺着进院”,术后3天即可撤机,7天即可站立行走
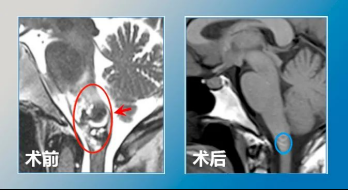
术后9月,复查MR显示病变全切,脑干组织复位等
总结:对于脑干海绵状血管瘤,一般以手术切除为根本治疗手段。反复出血是造成脑干以及脊髓等复杂位置海绵状血管瘤患者伤残和死亡的重要原因,部分切除的病例再出血可能性较大,可引起灾难性的神经功能缺失,顺利全切手术也是防止再出血以及患者获得治愈的根本方法。
参考资料:
- 1.DOI:https://doi.org/10.18791/nsatlas.v3.ch04.4
- 2.doi:10.1016/j.neuchi.2019.12.006

 胶质瘤
胶质瘤 垂体瘤
垂体瘤 脑膜瘤
脑膜瘤 脑血管瘤
脑血管瘤 听神经瘤
听神经瘤 脊索瘤
脊索瘤




 沪公网安备31010902002694号
沪公网安备31010902002694号