INC国际儿童脑瘤大咖、世界神经外科联合会(WFNS)执行委员会&顾问委员会成员之一的James T. Rutka教授发表研究《Therapeutic and Prognostic Implications of BRAF V600E in Pediatric Low-Grade Gliomas》(BRAF V600E在儿童低级别胶质瘤中的治疗及预后意义),以下是研究简述。
01. 目的
BRAF V600E是一种在儿童低级别胶质瘤(PLGGs)部分患者中检测到的潜在可高效靶向治疗的突变。其在这一多样化肿瘤群体中的生物学及临床效应尚不清楚。
02. 患者及方法
本研究为一项结合临床和遗传学的机构研究,纳入了接受长期随访的儿童低级别胶质瘤(PLGGs)患者(N = 510例)。对BRAF V600E突变型PLGG患者(n = 99例)的临床和治疗数据与一大型国际独立队列中BRAF V600E突变型PLGG患者(n = 180例)的数据进行了比较分析。
03. 结果
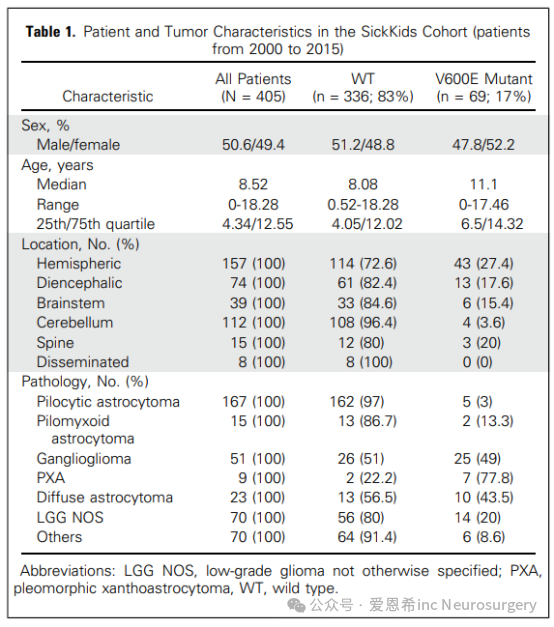
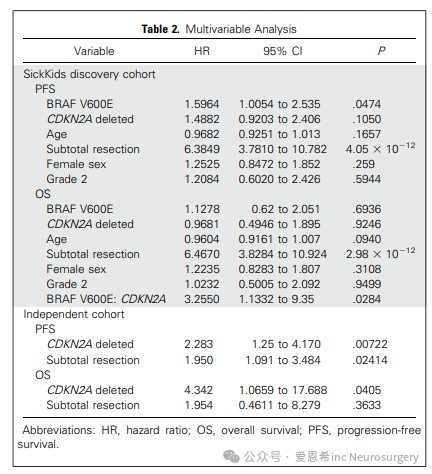
在405例儿童低级别胶质瘤(PLGG)患者中,有69例(17%)检测到BRAF V600E突变,这些突变出现在多种组织学类型和发病部位,包括临床上不常进行常规活检的中线位置。携带BRAF V600E突变的PLGG患者在化疗和放疗后的预后较差,导致BRAF V600E突变型和野生型PLGG患者的10年无进展生存率分别为27%(95% CI,12.1%至41.9%)和60.2%(95% CI,53.3%至67.1%)(P<.001)。进一步的多变量临床和分子分层分析显示,在BRAF V600E突变型PLGG中,切除范围和CDKN2A缺失是影响预后的两个独立因素。在独立队列中,CDKN2A缺失和切除范围对预后的类似独立影响也得到了观察。定量影像分析显示,大多数携带BRAF V600E突变的PLGG患者病情进展,且对传统化疗缺乏反应。
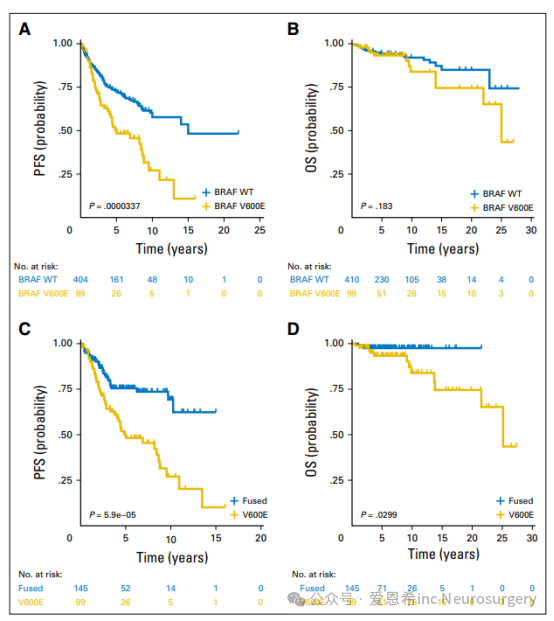
图1 儿童低级别胶质瘤患者按BRAF V600E状态分层的生存情况(SickKids队列)。
(A) 根据BRAF V600E状态的无进展生存(PFS)。
(B) 根据BRAF V600E状态的总生存(OS)。
(C) 比较BRAF V600E与KIAA1549-BRAF融合基因的无进展生存(PFS)。
(D) 比较BRAF V600E与KIAA1549-BRAF融合基因的总生存(OS)。
P值通过log-rank检验确定。
WT:野生型。
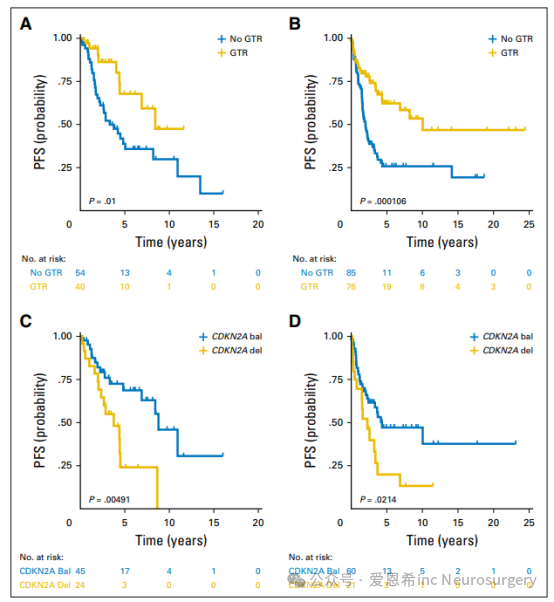
图2 BRAF V600E儿童低级别胶质瘤患者的生存情况根据切除范围和CDKN2A缺失状态进行分层。
(A) 根据切除范围的BRAF V600E SickKids队列的无进展生存(PFS)。
(B) 根据切除范围的BRAF V600E独立队列的无进展生存(PFS)。
(C) 根据CDKN2A状态的BRAF V600E SickKids队列的无进展生存(PFS)。
(D) 根据CDKN2A状态的BRAF V600E独立队列的无进展生存(PFS)。
P值通过log-rank检验确定。GTR:全切除。bal:平衡;del:缺失。
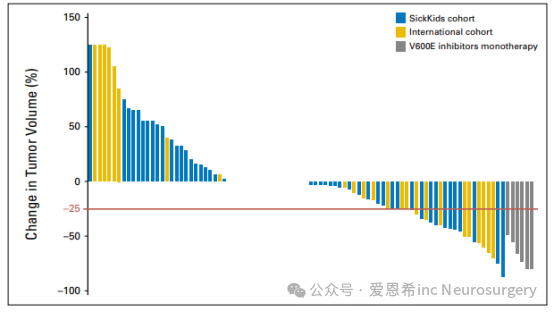
图3 BRAF V600E儿童低级别胶质瘤患者对化疗和BRAF V600E抑制剂的反应。瀑布图显示了患者在6个月时对化疗的反应。注意灰色部分表示对BRAF V600E抑制剂的反应。PFS:无进展生存。
04. 结论
BRAF V600E突变型儿童低级别胶质瘤(PLGG)在接受当前辅助治疗时表现为一种预后不良的独立疾病实体。

如果您也有想要分享的经历或者无法解答的疑惑,欢迎留言。

 胶质瘤
胶质瘤 垂体瘤
垂体瘤 脑膜瘤
脑膜瘤 脑血管瘤
脑血管瘤 听神经瘤
听神经瘤 脊索瘤
脊索瘤




 沪公网安备31010902002694号
沪公网安备31010902002694号