在大脑深处,有个比拇指稍大的器官叫做脑干,它几乎管辖着生命的一切,如呼吸、心跳、意识等。相比较大脑其他部位,脑干因其特殊的解剖位置和重要的生理功能,长期以来被称为“手术禁区”。能闯进这个“禁区”,并不断完成一个个挑战的医生,需要神经外科医生具有高超的技术、丰富的成功临床经验,稍有闪失,患者将出现呼吸循环衰竭、肢体瘫痪等并发症,长期卧床、呼吸机辅助呼吸等生命风险。
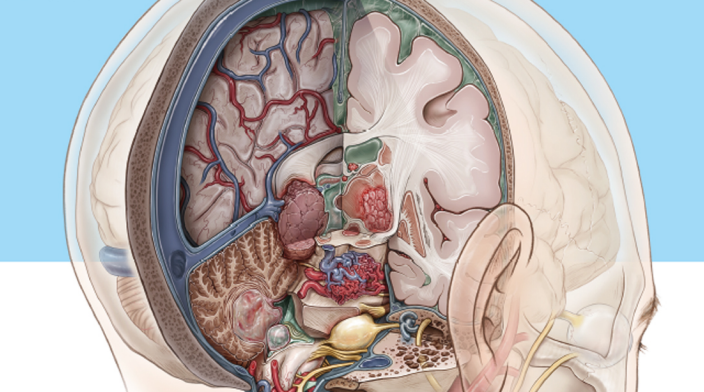
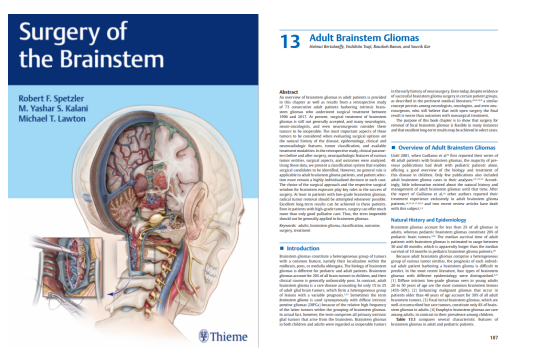
图自《Surgery of the Brainstem》
髓帆入路全切脑干胶质瘤案例一则
20岁的女孩Lea美丽自信,然而,急性头痛却扰乱了她的生活。极度的头痛吃药也无法缓解,随即到当地的医院进行检查。诊断结果是由于背侧外生的中脑肿瘤引起的梗阻性脑积水而极度头痛。专家给出的意见是手术风险太大,没有意义,建议保守治疗。保守治疗后,症状无明显改善,Lea不甘心,在医生的介绍下咨询德国巴特朗菲教授。
从磁共振影像来看,可能患的是高级别胶质瘤。如果真是这样,Lea的生存期不会超过一年。单从片子来看,瘤子位置确实深,而且累及中脑和上脑桥。手术中稍不注意,或者损伤中脑患者变成植物人,损伤桥脑引起半身瘫痪,严重损伤延髓影响呼吸功能。然而,巴特朗菲教授给出了不一样的意见:“由于患者没有神经功能缺损,且肿瘤呈外生性生长,肿瘤高度恶性似乎不太可能,并与患者及其家人讨论了Lea的脑瘤可能是低级别胶质瘤。需要结合这个肿瘤生长方式的特点,手术可以达到近全切或者全切的效果,可以明显改善巨大肿瘤占位引起的脑干和小脑压迫效应,从而明显改善症状、延长生存期。”
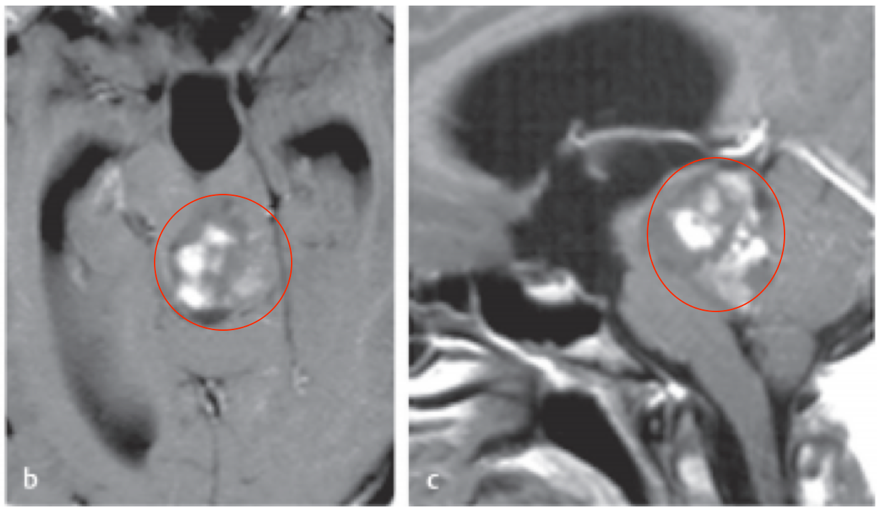
图:术前增强MRI提示脑干巨大占位,高级别肿瘤累及中脑和上脑桥。
手术过程
术者:INC德国巴特朗菲教授及其治疗团队。
诊断:脑干中脑背侧外生型胶质瘤
术中:半在整个手术过程中持续术中电生理监测,监测经食管超声心动图,以早期发现可能的空气栓塞。进行了枕下正中大骨瓣开颅术,肿瘤通过第四脑室经髓帆入路进入。根据术中菱形窝定位,肿瘤位于左侧面神经丘上方。由于肿瘤与周围的脑干实质有很好的边界,术中肿瘤全切,术后MRI复查明确未见肿瘤残余。
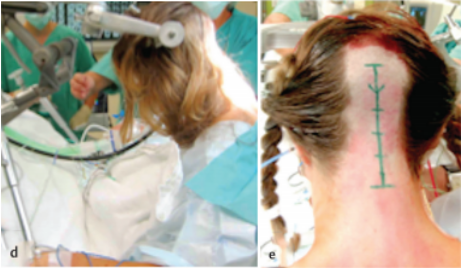
图:术中半坐位、术中电生理持续监测下经髓帆入路全切肿瘤。
术后情况
术后运动功能完好,仅出现轻度的第六神经麻痹引起轻微的半侧面部感觉麻痹和轻微的复视,术后两个月症状明显缓解。组织病理学检查为WHO1级毛细胞星形细胞瘤。巴教授结合手术中情况和病理结果,表示1级胶质瘤且肿瘤全切,术后无需辅助放化疗,注意随访观察即可。她的后续康复良好,术后多次MRI检查均未发现局部肿瘤复发或其他颅内异常。
术后11年随访:术后MRI显示患者没有肿瘤残留或复发。患者的临床状况良好,眼球运动正常。
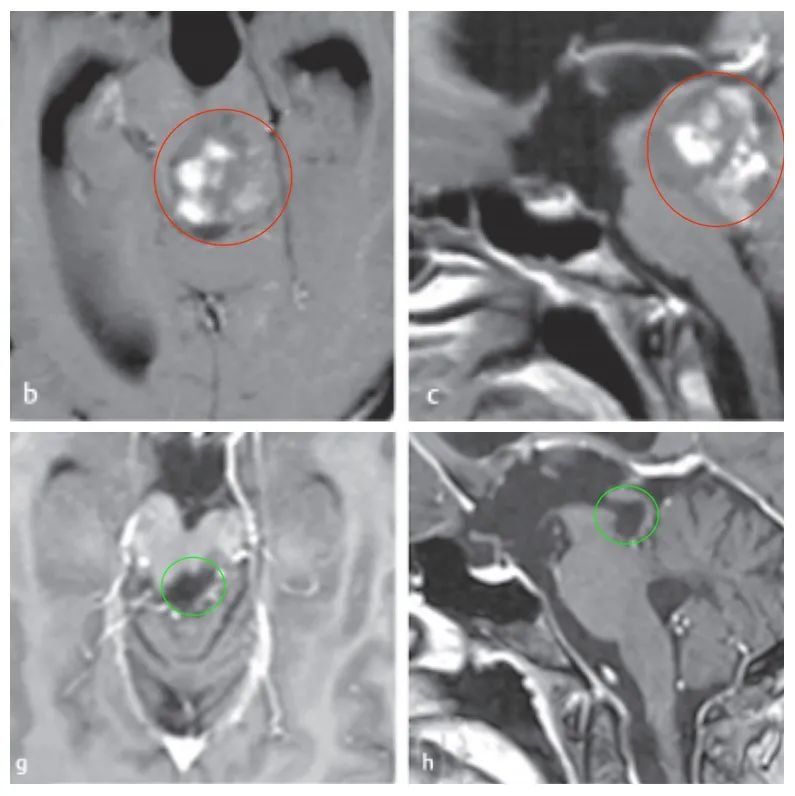
图:术前术后脑磁共振对比,脑干胶质瘤全切,无神经脑组织损伤。

图:显示肿瘤全切除术后11年的随访中,患者状态良好,无肿瘤复发。
该案例来源于2020年新版的世界脑干手术专著《Surgery of the Brainstem》(脑干手术)中,巴特朗菲教授撰写的《adult brainstem glioma》(成人脑干胶质瘤)章节。该章节回顾性研究了1996年至2017年间接受手术治疗的73例患有脑干神经胶质瘤的成年患者。重点详细阐述了脑干手术的技术要点、操作技巧、手术入路、手术体位等,已成为神经外科医生的学习典范。
哪些脑干胶质瘤可以手术?
手术原则是在保护功能的前提下最大程度地切除肿瘤,以延长患者的生存期;部分有脑积水或颅高压症状但不适宜肿瘤切除的患者可选择减压术、分流术缓解症状。除以下所列的适应证外,最终是否采取手术治疗需结合病情的轻重、进展速度、患者的一般情况及意愿进行综合考虑。
临床中,一般如下患者有手术适应证:
① 外生型BSG。
② 局灶内生型BSG。
③ 伴有局灶性强化或11C-MET PET-CT显示伴有局灶高代谢的弥散内生型BSG。
④ 不伴有局灶性强化或11C-MET PET-CT成像显示不伴有局灶性高代谢的DIPGs可选择开放活检术或立体定向活检术。
⑤ 观察期间表现出恶变倾向的胶质瘤(体积变大、MRI增强扫描出现强化、侵及周围结构)。
注:虽然这些情况时具有手术适应症指征,但手术风险大,仍需全面权衡手术获益和致残风险,尽量需求具有较多同类成功手术经验的医师团队至关重要。
不适应手术的情况有如下
① 弥散型BSG累及整个脑干(中脑、脑桥、延髓)。
② 伴有软脑膜播散或种植的BSG。
③ Karnofsky功能状态评分(KPS)<50分,脑干功能严重衰竭的患者。
④ 合并多脏器功能异常,无法耐受手术者。
手术方案的制定:
不同部位的BSG常用的手术入路见表2.脑干安全进入点的选择至关重要,建议在纤维束导航及术中神经电生理监测的引导下避开脑干内重要的传导束和核团,选择脑干表面离肿瘤最近的区域进入,应沿纤维束走形方向切开脑干,避免对纤维束过多的损伤。术中尽可能减少对脑干的机械牵拉,尽可能避免对脑干正常供血动脉和引流静脉的损伤。

表2.不同部位脑干胶质瘤采用的手术入路
脑干长期被视为“手术禁区”,随着显微神经外科技术、术中辅助技术发展及脑干安全区的发现,直到如今依然仅有少数手术医生有较多成功的手术报道。小小的脑干位处大脑深处,手术入路的选择对脑干病变手术仍至关重要,临床常见脑干病变术后发生严重的并发症,有些是可以通过改进手术入路而避免并且达到最佳的肿瘤切除效果,合理的选择个体化的手术入路治疗脑干病变至关重要,这就需要术者对脑干的解剖基础、肿瘤生长特点有深入了解及对丰富的各种手术入路经验。
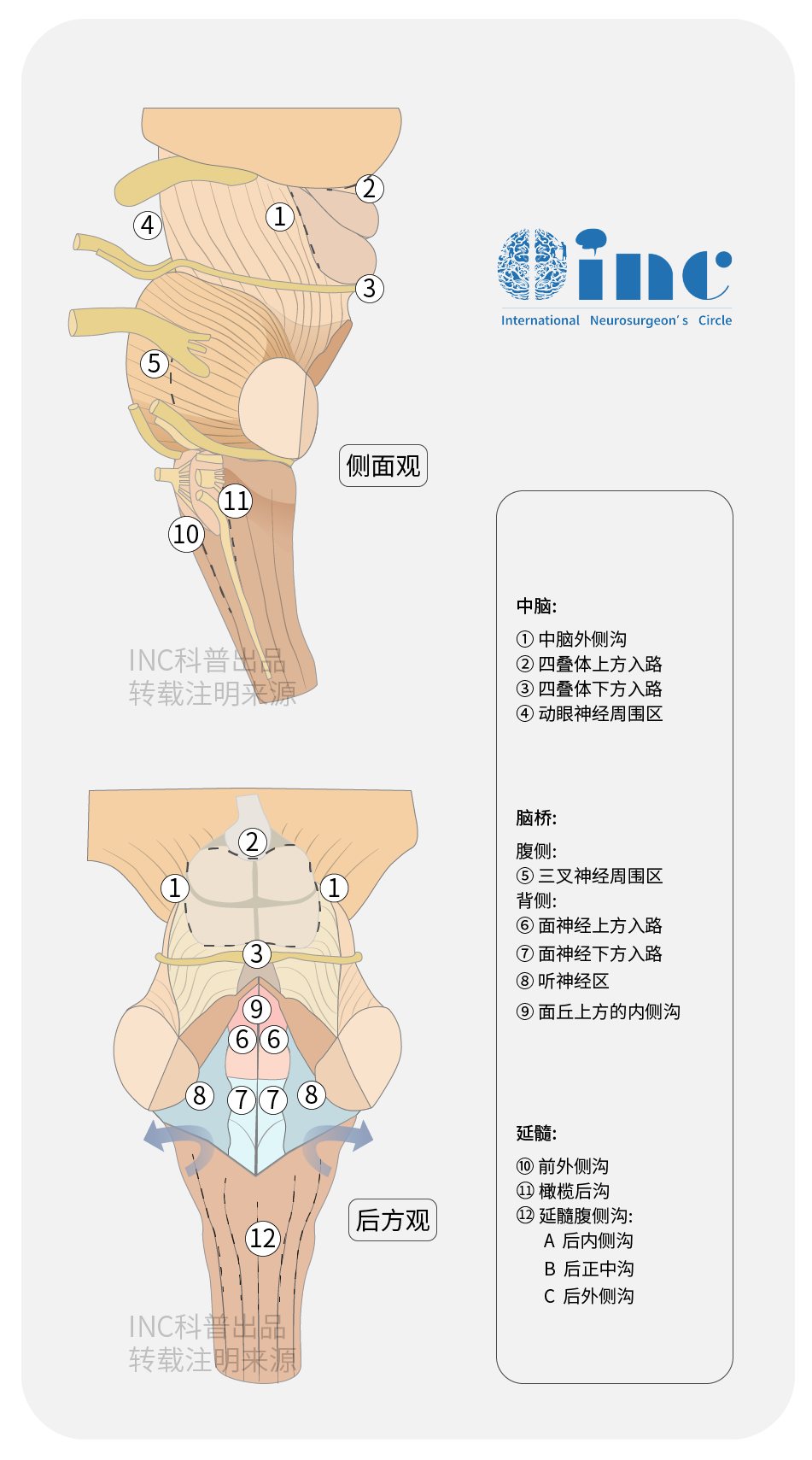
脑干安全区
如何一举歼灭脑干胶质瘤?
1、手术指征和手术入路
在脑干肿瘤手术中,重要的是确定正确的手术指征。因此,要选择真正符合条件的患者, 你不想让手术对病人造成比肿瘤更大的伤害。因此,在许多脑干胶质瘤手术中,我们不能假定可以实现完全切除。我们必须确定手术的目标,并与家属和成年患者明确沟通,说明什么是可行的,什么是安全可行的。
我们当然可以切除一切,但在很多病例中,我们不想损害神经功能。当然,手术时机和手术入路也很重要,因为在脑干的各个区域,我们只有一个很小的窗口来暴露肿瘤,然后我们需要知道从哪一侧,幕上还是幕下等等,以确定我们需要暴露肿瘤的确切入路。手术技术在脑干内部也发挥着重要作用。脑干胶质瘤位置的分布与海绵状血管瘤完全不同,后者多位于脑桥,而胶质瘤多位于中脑。
2、自然间隙微创手术
巴教授善于用无热能、钝性工具,如显微镊、神经剥离弯钩等去钝性分离肿瘤薄膜及瘤外正常组织和神经结构。显微CUSA无牵拉的瘤内减压、切瘤,再慢慢把这包膜剥掉,尽量从脑组织的自然缝隙通道中,把瘤子从一众神经血管丛林中分、剥、切出来,并且很好地利用“打水Irrigation”等操作,避免手术中各种器械来回折腾、热损伤、操作物理损伤等。
“打水Irrigation”充分发挥了水和重力的物理原理,让水的重量产生恰到好处的力去分离组织,利用体位优势让术野积水积血自然流出等,尽量做到“不出血、不碰神经、不电凝肿瘤、不电凝血管神经”。
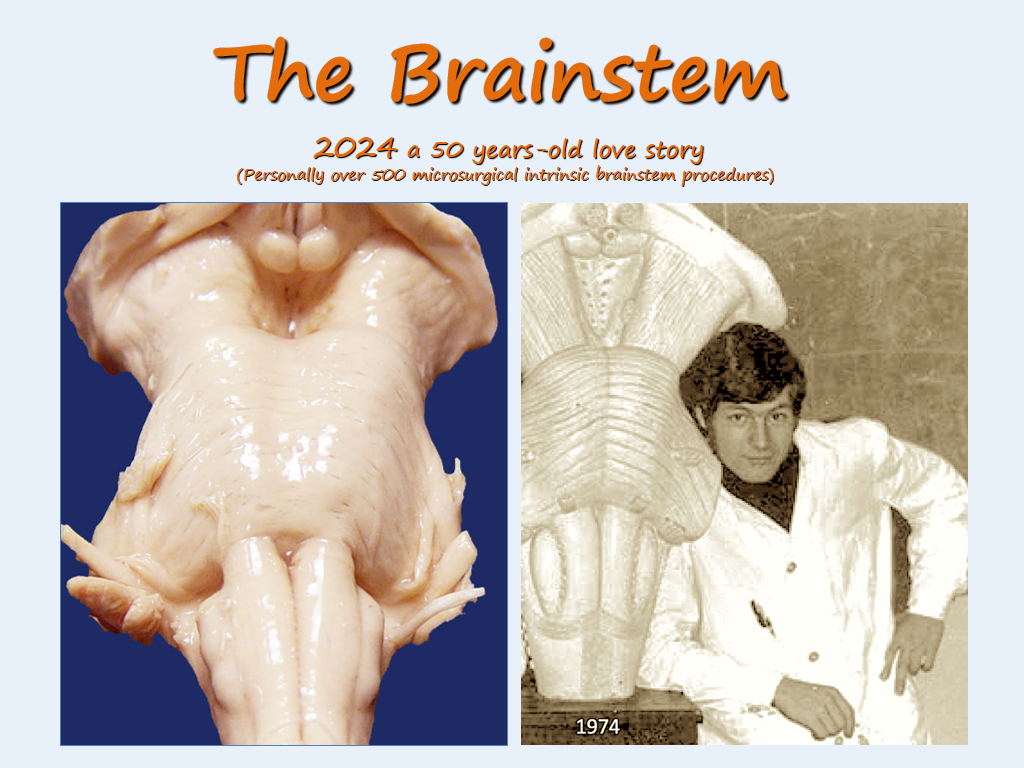
▼巴教授对于脑干手术解剖的深入了解源于携手脑干50年的“love story”,点击图片了解
3、显微“冷刀”手术理念
巴教授优先使用无热能器械和钝性分离技术,避免热损伤与血管痉挛。显微镊与神经剥离弯钩:沿肿瘤包膜与脑组织的界面,轻柔钝性分离,逐步推开粘连的神经血管结构(如穿支动脉、静脉)。适用肿瘤包膜完整、与周围组织粘连紧密(如脑膜瘤、神经鞘瘤)。
巴教授借助CUSA刀进行肿瘤切除,显微CUSA无牵拉的瘤内减压、切瘤,尽量从脑组织的自然缝隙通道中,把瘤子从一众神经血管丛林中分、剥、切出来。切除肿瘤时需谨慎,避免打穿瘤壁,以防损伤粘连的神经和血管。
4、术中神经电生理监测
这被誉为”神经外科医生的第三只眼“,为了保障艺文术后的生活质量,这一台手术也是如常使用,双侧MEP和SEP(分别监测运动传导功能和感觉传导功能)。巴教授认为如果脑外科手术没有电生理监测,那是不人道的。因为手术中进行神经电生理监测,就像安装了“报警器"一样,医生下刀前,通过监测器的微电流刺激,如果会伤到重要的神经,监测器就会发出警报,那么这一刀就不开下去了,避免了误伤。
脑干手术对神经外科医生来说是一个巨大的挑战,但影像学、手术方法和术中神经生理监测的进步降低了与这些手术相关的风险和发病率。有或无外生成分的局灶性内生脑干肿瘤和原发性外生病变可以通过手术切除。尽管脑干手术的显微外科技术已经取得了进展,但这些技术的持续发展仍需要为患者提供尽可能好的护理,致力提高患者的生活质量。

巴教授作为世界神经外科联合会(WFNS)教育与技术委员会前主席,专研脑干、脊髓、颅底、丘脑等疑难位置神经外科疾病手术,是名副其实的“国际颅底、脑干肿瘤手术大咖”,国内患者尊称他为“巴教授”。近40年,数千台疑难神经外科疾病手术,巴教授历经千万个小时用超精确的物理剥除诠释了医术为何为艺术。


 胶质瘤
胶质瘤 垂体瘤
垂体瘤 脑膜瘤
脑膜瘤 脑血管瘤
脑血管瘤 听神经瘤
听神经瘤 脊索瘤
脊索瘤




 沪公网安备31010902002694号
沪公网安备31010902002694号